在呼吸過程中交換氧氣和二氧化碳的肺部組織「肺泡」是位於支氣管末端的一種細小囊狀結構,成人肺中的肺泡數量可達數億個之多。如果罹患慢性阻塞性肺病(COPD、慢阻肺)之類的嚴重肺部疾病,肺泡可能會遭到破壞,從而導致呼吸困難甚至死亡。然而,到目前為止,再生破損肺泡的方法還未確立。
肺泡的形成需要具有較強收縮力的肺泡肌纖維母細胞的參與。根據既往研究結果,研究人員提出了肺泡肌纖維母細胞纏繞在囊狀的終末囊泡上,通過收縮形成窄口,從而形成肺泡的模型。此次,日本醫科大學先端醫學研究所病態解析學部門的高野晴子教授和該大學研究生院福原茂朋教授等組成的研究團隊著眼於構成肺泡的細胞之一、負責氧氣和二氧化碳等氣體交換的血管內皮細胞,在破壞了該細胞内信號分子「Rap1基因」的小鼠體內,成功發現了肺泡的形成受到了抑制的現象。
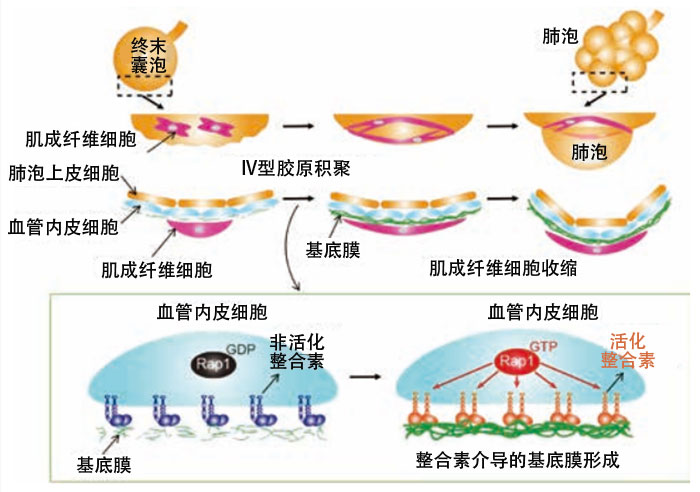
研究發現,血管內皮細胞具有通過激活細胞粘附因子「整合素」,積聚Ⅳ型膠原蛋白,形成充當肌纖維母細胞支架的基底膜,誘導肌纖維母細胞收縮,從而促進肺泡形成的作用。
這個研究結果表明,血管內皮細胞在Rap1蛋白的作用下,通過激活細胞粘附因子「整合素」並積聚Ⅳ型膠原蛋白形成基底膜,基底膜起著肌纖維母細胞支架的作用,誘導肌纖維母細胞收縮,進而促進了肺泡的形成。
應用本次研究成果,如果能開發出肺泡再生技術,便有可能為COPD(慢阻肺)和感染性呼吸道疾病等提供新的治療方法。此外,在試管中模擬臟器功能製成的肺泡類器官中,通過融合此前未曾包含的血管內皮細胞,能夠增加類器官的功能,有望為闡明疾病原因和開發治療方法做出貢獻。(TEXT:原 繪里香)
原文:JSTnews 2024年6月號
翻譯:JST客觀日本編輯部














