東海大學理學部化學科的荒井堅太副教授、岩岡道夫教授與山梨大學醫學部婦產科學講座的吉野修教授、小野洋輔臨床助教等人組成的合作研究團隊,首次成功化學合成了人們熟知的妊娠激素「人鬆弛素2(relaxin)」中的兩種人工鬆弛素(硒鬆弛素、Serenorelaxin),三對雙硫键中的一對置換為了類似二硒鍵。此外研究表明,單獨一種硒鬆弛素最多可將一種被認為與子宮內膜異位症發病有關的組織纖維化因子——「PAI-1」的mRNA表達量減少至原先的40%。這個研究成果明確了使用二硒鍵置換雙硫键的分子設計能夠提高鬆弛素合成效率,同時為子宮內膜異位症的新藥開發戰略提出了一種新方案。研究成果已發表在期刊《RSC Chemical Biology》的電子版上。
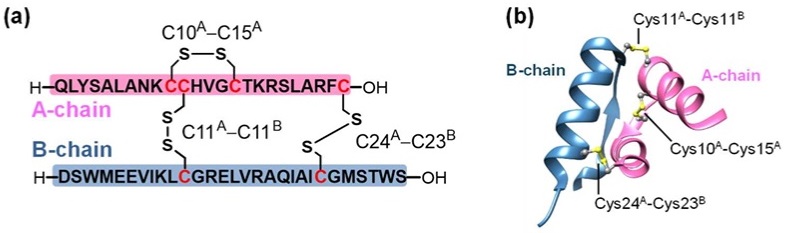
圖1鬆弛素的結構(a):通過三對雙硫键偶聯的鬆弛素A鏈和B鏈的胺基酸序列。大寫字符示氨基酸的種類。(b)鬆弛素的三維結構(蛋白質數據庫碼PDB code:6rlx)(供圖:東海大學)。
罹患子宮內膜異位症的女性約佔育齡婦女的10%,該病可誘發痛經、性交疼痛和排便障礙等症狀,顯著降低女性的生活品質(QOL)。合作研究團隊曾於2020年報告稱,鬆弛素可能對子宮內膜異位症具有緩解作用。
鬆弛素是一種分子量約6000的蛋白質,由A鏈(24個胺基酸殘基)和B鏈(29個胺基酸殘基)兩條多肽鏈組成,其分子結構通過A鏈和B鏈之間形成的兩對雙硫键(S-S)以及A鏈内部形成的一對雙硫键來保持穩定。
在兩種不同物質之間選擇性地形成鍵合在技術上十分困難。儘管鬆弛素是一種在新藥研發領域極為重要的蛋白質,但其化學合成方法至今尚未確立。
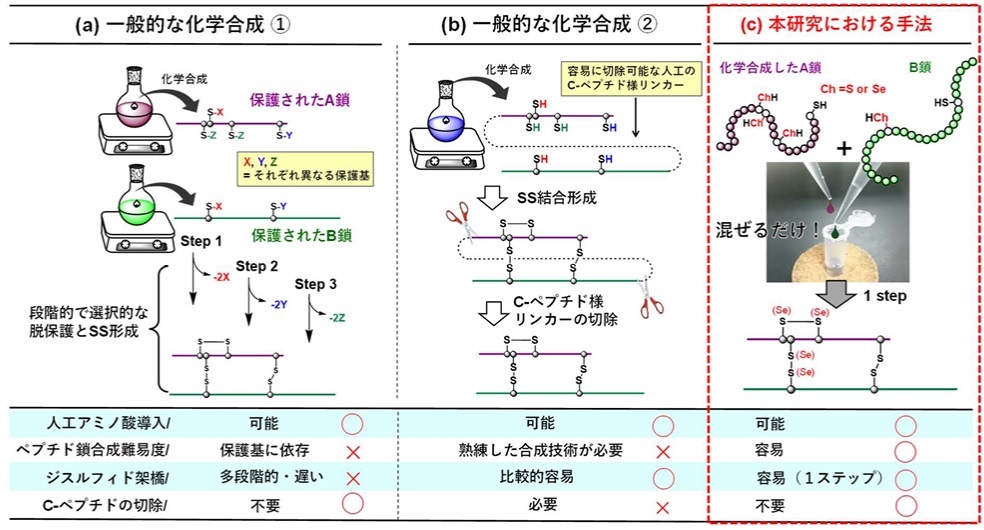
圖2鬆弛素的化學合成示例。(a)通過多種保護基團的選擇性脫保護以及雙硫键交聯合成鬆弛素。(b)通過模擬生物合成機制的單鏈鬆弛素前驅物合成以及雙硫键交聯合成鬆弛素。(c)利用本研究中確立的高反應性硒原子(Ch=Se)實現鬆弛素結構肽鏈的直接偶聯。(供圖:東海大學)
本次研究中,東海大學的團隊應用了以往用於化學合成與鬆弛素結構相似的胰島素的技術,通過在適當的添加劑存在下,將原料的鬆弛素A鏈和B鏈以適當的組合方式進行混合,成功地一次性獲得了目標物質的各種鬆弛素類似物。
不具有二硒鍵的野生型鬆弛素48小時後能夠以47%的產率獲得目標物質鬆弛素,而用二硒鍵置換了暴露在鬆弛素分子表面的雙硫键的「硒鬆弛素α」則大幅提高了A鏈和B鏈的偶聯產率,72小時後能夠以73%的最高產率獲得目標物質。另一方面,用二硒鍵更換鬆弛素分子内部雙硫键的「硒鬆弛素β」的最高產率為34%,略低於野生型,但其反應是在24小時内完成的。
也就是說,研究發現分子表面的二硒鍵和分子内部的二硒鍵分別控制了偶聯的產率和速度。此外,對偏析出的各種鬆弛素和硒鬆弛素的結構分析結果提示,本次研究團隊試圖合成的兩種硒鬆弛素都具有與野生型鬆弛素相似的結構。
研究團隊此前曾發現,來自子宮內膜異位症患者的子宮內膜間質細胞中普遍存在著鬆弛素的接受者——富含白胺酸的G蛋白偶聯接受者7(LGR7),而鬆弛素可以作為子宮內膜異位症的抑制劑發揮治療作用。因此,本次研究團隊針對合成硒鬆弛素對子宮內膜間質細胞的作用展開了研究,並重點討論了該物質對纖溶酶原/酵素原激活物抑制因子-1(PAI-1)的表達抑制作用。
研究結果提示,PAI-1在組織纖維化過程中起到重要作用,子宮內膜異位症患者腹腔液中高濃度的PAI-1參與了腹膜病灶的發病。在使用合成鬆弛素(100納克/毫升)進行處理的所有實驗組中,PAI-1的mRNA表達均發生了統計學意義上的顯著減少。與野生型鬆弛素相比,兩種合成的硒鬆弛素能更有效地抑制PAI-1的mRNA表達。低濃度(33納克/毫升)情況下,硒鬆弛素β在該測定中表現出的有效性最高。這些實驗結果顯示,從抑制PAI-1產生的角度看,硒鬆弛素可能對子宮內膜異位症具有較高的抑制效果。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:RSC Chemical Biology
論文:Seleno-relaxin analogues: effect of internal and external diselenide bonds on the foldability and a fibrosis-related factor of endometriotic stromal cells
URL:pubs.rsc.org/en/content/articlelanding/2024/cb/d4cb00095a













