岡山大學等的研究團隊開發出一種在外科手術中可以輕鬆連接或剝離器官的粘合劑。目前,器官的連接主要採用縫合的方法,而此次新開發的粘合劑可以在沒有高超技術的情況下快速完成粘合,如果通過大量注水,還可在不傷害組織的情況下剝離。該技術實用化後,不僅能縮短手術時間,還可能用於下一代體內植入型器件的固定和拆卸。
岡山大學學術研究院醫齒藥學域(牙科)生物材料學領域的松本卓也教授等人組成的研究團隊為瞭解決在手術過程中把器官貼合在一起或固定在一起以確保視野的問題,設計了這款材料。縫合不僅費時,而且依賴於外科醫生的技術水平。恢復後還需要拆線,處理繁瑣。作為不縫合的方法,雖然已有一種名為「纖維蛋白膠」的組織粘合劑,但需要花費時間才能粘合,且粘合力較弱。
松本教授等人為了開發高實用性的新型粘合劑,著眼於骨骼形成的過程。在骨骼形成過程中,骨端的軟骨細胞的活動變得活躍,附近的球狀礦物質相互粘合形成骨骼。在此過程中,這些礦物質利用周圍的膠原蛋白組織作為「粘合劑」。松本教授發揮逆向思維,認為如果能夠巧妙地將骨成分作為粘合劑使用,那麼它可能會粘附在含有大量膠原蛋白的器官表面。
研究小組於利用骨和牙齒的主要成分——磷酸鈣(羥基磷灰石)粉末,將其製成微細奈米顆粒(1奈米為十億分之一米),然後經過模製和高溫燒製處理,便形成了許多粒子之間存在小空隙的打孔分佈板。最終開發出邊長約5毫米的無機陶瓷類粘合劑。磷酸鈣通過吸收生物組織中的水分,吸引並粘附器官中的膠原蛋白成分,隻需輕壓就能粘合。

此次開發的用於器官的磷酸鈣粘合劑。邊長5毫米,排列多個使用可以提高強度(圖片由松本卓也教授提供)。
新型粘合劑在幾乎沒有水分的角質層中無法粘附,但在真皮和器官上能有效粘合,因此在手術中可以方便地使用。對於其機制,松本教授解釋說:「就像用米飯當漿糊時一樣。當完全沒有水分或水分過多時就無法粘附,而在水分適中時,就會有粘性。」已證實,這種粘合劑的粘合力是纖維蛋白膠的三倍。
粘合劑在形成過程中,燒製溫度的變化會導致磷酸鈣的密度發生變化。研究小組發現,在600℃左右時,粘合力保持穩定,但溫度進一步升高會導致粘合力下降。這是因為密度變化會影響多孔質的孔大小。調節水分的含量,被認為能影響粘合力的強弱。利用上述溫度差,可以針對需要蠻力粘合的物品和要求弱粘合性的物品分別控制對應。此外,大量注入水分就能使其失去粘合力並剝離。
研究小組使用豬肝進行了實驗,以檢驗粘合劑是否在實際器官中有效。實驗中,將9個粘合劑排放在一塊黏扣帶的背面,確認它們能夠粘附,並通過加水確認剝離,證明了粘合劑的功能。此外,研究人員還對組織標本進行了檢查,發現器官沒有受到傷害,也沒有出現有害副作用。粘合劑在消毒清洗後也不會損壞。今後,將以應用於人體為目標繼續開展實驗。
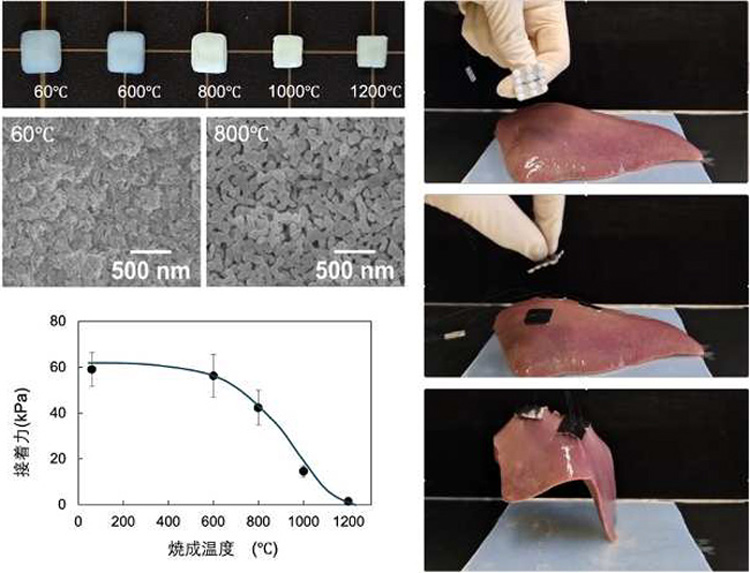
使用豬肝進行的粘合實驗(右邊照片)。燒製溫度超過600度時,粘合力會下降。利用此現象,可以控制粘合的強弱(圖片由岡山大學提供)
在瑞典,有越來越多的人將微晶片植入體内用於支付等目的。嵌入體內的晶片需要足夠小,並且要防止在體內移動。松本教授表示:「正如(美國企業家)埃隆·馬斯克的公司Neuralink正在開發腦内植入型設備一樣,我認為未來人類體內植入型設備將會普及。如果此次開發的粘合劑能夠用於人體,就可以使這種設備的固定和拆卸變得容易。此外,我認為它也可以應用於寵物用的微晶片。」
該研究得到了日本學術振興會科學研究費助成事業的認定和日本科學技術振興機構(JST)的戰略性創造研究推進事業「CREST」的資助。相關論文於5月1日發表在美國科學期刊《Advanced Healthcare Materials》的電子版上,岡山大學也於同月24日發布了相關成果。
【論文資訊】
發表期刊:Advanced Healthcare Materials
論文標題:Water-mediated on-demand detachable solid-state adhesive of porous hydroxyapatite plate for organ retractions
DOI: 10.1002/adhm.202304616
原文:JST Science Portal 編輯部
翻譯:JST客觀日本編輯部
【相關鏈結】
岡山大學新聞稿「開發出可黏著剝離器官的粘合劑!有望簡化手術程序」
「Neuralink」官方網頁














