熊本大學發育醫學研究所的古賀沙緒裏助教和小川峯太郎教授的研究團隊發表研究成果稱,成功在試管中將造血幹細胞的祖細胞——血管內皮細胞誘導分化成為了造血幹細胞。研究團隊通過再現由血管內皮細胞分化造血幹細胞的發育過程所需環境,獲得了上述成果。由於無需基因改造或添加血清等,這種方法具有高的通用性,因此有望成為明確造血幹細胞發育的詳細機制的強大工具。相關成果已發表在《美國國家科學院院刊》(PNAS)7月23日號上。
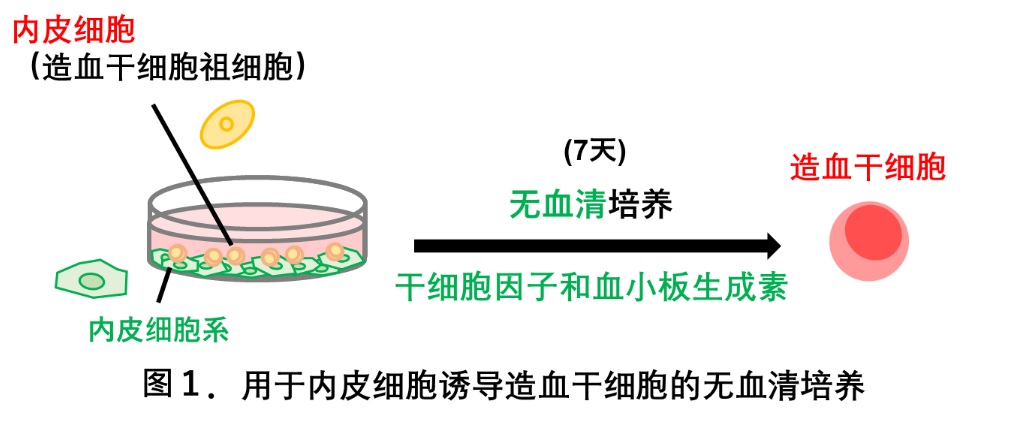
造血幹細胞存在於骨髓中,能夠不斷自我克隆並產生血液細胞。如果這些細胞出現問題或發育過程中發生基因異常,則會導致血液病。
因此,如果能在試管中再現造血幹細胞的正常發育過程,將有望通過研究基因突變的影響揭示疾病的原因。
另一方面,既往研究中在試管中從血管內皮細胞分化造血幹細胞時,需要與經過基因改造的支持細胞共同培養,或在有血清存在的情況下培養。但由於這種方法通用性較低及血清中細胞介素等的影響,阻礙瞭解明機制的進程。
本次研究人員旨在克服這些問題,構建一種僅使用通用材料的無血清造血幹細胞分化誘導方法。
造血幹細胞是胚胎期主動脈内的血管內皮細胞通過前造血幹細胞發育而成的。
研究人員在小鼠胚胎體內探索了前造血幹細胞表達的信號因子接受者,並發現其中表達了SCF(幹細胞介素)接受者KIT和TPO(血小板生成素)接受者MPL。
在無血清培養液中培養前造血幹細胞時,研究人員通過添加SCF和TPO,使其分化為了造血幹細胞,而單獨添加任何一種都不會導致分化。
研究團隊進一步探索了血管內皮細胞分化為造血幹細胞的條件。結果發現需要添加血管內皮細胞株作為血管內皮細胞的支持細胞。
胚胎體內血管內皮細胞發育的主動脈腔主記憶體在SCF,但不存在TPO。
由於TPO隻由肝母細胞產生,研究發現,前造血幹細胞從主動脈腔内遷移到肝臟後,接受TPO信號後才能分化為造血幹細胞。
古賀助教表示:「本研究中確立的培養方法隻使用了全球研究人員都能簡單獲取的研究工具,因此有望成為詳細研究造血幹細胞發育過程的標準方案。 今後,我們的目標是建立從富潛能幹細胞到造血幹細胞發育過程的再現培養技術。並將致力於開展能夠對醫學領域做出貢獻的研究,如再生醫學的應用和疾病原因的闡明等」。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Proceedings of the National Academy of Sciences of the United States of America (PNAS)
論文:Transition of signal requirement in hematopoietic stem cell development from hemogenic endothelial cells
DOI:10.1073/pnas.2404193121













