日本東北大學的小關良卓助教和笠井均教授等人改良了已投入實際使用的抗癌藥物的結構,使其在癌細胞中更容易產生作用。藥物在癌細胞中含有的某些物質產生作用時,結構會發生變化,從而產生效果。動物實驗證實,這種改良後的藥物比現有藥物能更有效地抑制癌細胞的生長。今後,研究團隊還將推進安全性驗證,並進行臨床試驗,將副作用更小的抗癌藥物投入臨床。
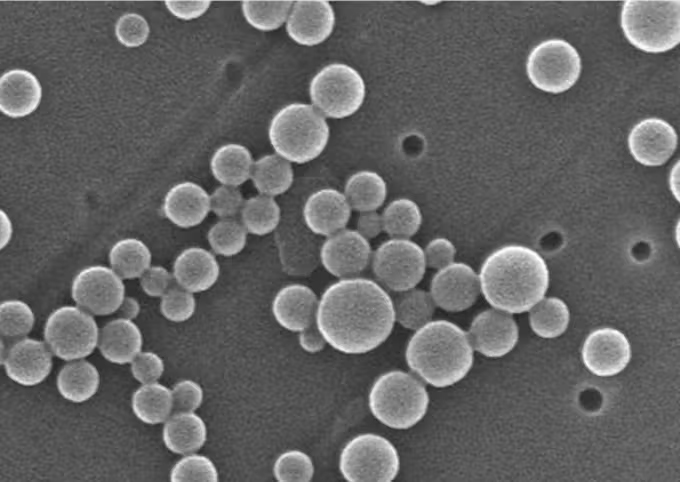
對已投入實際使用的抗癌藥物進行了結構改良(新結構藥物的電子顯微鏡照片)(供圖:東北大學小關良卓助教)
研究團隊改進了具有抗癌作用的物質「SN-38」。這種物質能干擾細胞克隆DNA並抑制細胞分裂。由於原本的結構難溶於水,所以難以作為藥物使用,而是將改變了部分結構的「伊立替康」作為藥物使用。當肝臟中的酶開始作用時,藥物就會開始作用。
但是「伊立替康」對癌細胞以外的細胞的影響沒有得到充分的抑制,會導致腹瀉等強烈的副作用。研究團隊著眼於癌細胞含有大量名為麩胱甘肽的抗氧化物質,將兩個SN-38分子通過化學鍵連接起來,當麩胱甘肽發揮作用時,化學鍵會斷裂,SN-38分子開發端揮作用。將這種通過化學鍵連接起來的SN-38分子投餵給患有癌症的小鼠後,發現其對抑制癌症增殖的效果優於伊立替康,且未觀察到嚴重的毒性。
麩胱甘肽僅少量存在於血液中。使用新結構的SN-38分子時,血液中幾乎不出現SN-38,而在癌細胞中則會大量生成,因此副作用的發生率較低。雖然也有麩胱甘肽含量不高的癌細胞,但通常來講,癌細胞中的麩胱甘肽含量要高於正常細胞。
研究團隊今後的目標是開發出達到符合藥品標準的品質,再次驗證其安全性等,計劃在5至10年内啟動臨床試驗。相關研究成果已經發表於英國科學雜誌《Nanoscale》上。
原文:《日本經濟新聞》、2024/9/3
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Nanoscale
論文:Carrier-free Nano-prodrugs for Minimally Invasive Cancer Therapy
DOI:10.1039/d4nr01763c













