東京大學等研究團隊發現,通過向在癌症放射線治療中被認為實用性較低的對映異構體硼化合物添加液體膠成分,較現行臨床中使用的藥物更容易聚集並停留在癌細胞中。研究團隊利用加速器硼中子捕獲療法(BNCT)成功使小鼠體內的癌症基本消失。今後,研究團隊計劃將其應用於人類的胰腺癌等難治性癌症上。
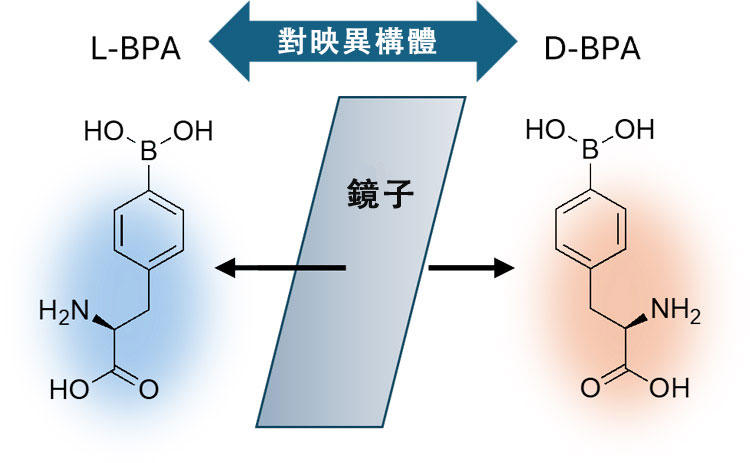
加速器硼中子捕獲療法 (BNCT) 中使用的L-L-硼醯基苯丙胺酸(L-BPA,左)的對映異構體D-BPA(D-BPA,右)和聚乙烯醇(PVA)結合後,藥物更容易聚集和停留在癌細胞中(供圖:東京大學野本貴大副教授)
BNCT是通過低能量熱中介子與硼原子碰撞,在約一個細胞大小的範圍內產生輻射來殺死癌細胞的放射治療方法。該療法已在2020年被批准適用於某些無法手術切除的頭頸部癌症。目前,基於其較強的癌細胞吸收性,臨床上主要使用L-硼醯基苯丙胺酸(L-BPA)作為藥物。
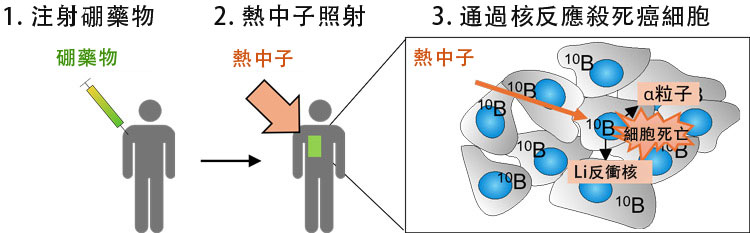
BNCT原理概述。通過注射硼苯丙胺酸(BPA)並用加速器等產生的熱中介子照射來殺死含有BPA的細胞(供圖:東京大學野本貴大副教授)
L-BPA可通過被癌細胞特有的轉運體獨特性地吸收達到臨床所需的濃度,並在熱中介子照射下殺死癌細胞。然而,該方法也存在一些限制其效果的問題,例如被吸收後如果時間過長,會通過轉運體釋放到細胞外,或通過其他的轉運體進入正常細胞等。
研究將藥物輸送到體內特定部位的藥物靶向遞送技術的東京大學研究生院綜合文化研究科的野本貴大副教授提出了「是否能讓L-BPA更有選擇性地被癌細胞吸收,並長時間停留在細胞內?」的想法。2020年研究團隊通過在L-BPA中加入一種在液體膠中使用的聚乙烯醇(PVA)後,發現可以促使癌細胞通過膜內凹形成的囊泡更加容易地吸收藥物。研究團隊推測,將難以被癌細胞吸收且此前認為對癌症治療無用、與L-BPA結構上如左右手般對稱的對映異構體D-BPA,如果能與PVA結合使用,可能對癌症治療同樣有效,為此開始了相關實驗。
研究發現,當將D-BPA與PVA共同作用於小鼠大腸癌及來源於人類胰腺癌的培養細胞時,與L-BPA一樣,D-BPA通過囊泡更容易被癌細胞吸收。此外,通過動物實驗觀察藥物在癌細胞中的濃度發現,與L-BPA相比,D-BPA在癌細胞中可以維持較高濃度更長時間。野本副教授分析原因表示,這可能是因為D-BPA不像L-BPA那樣會通過運輸體從細胞內流出的緣故。
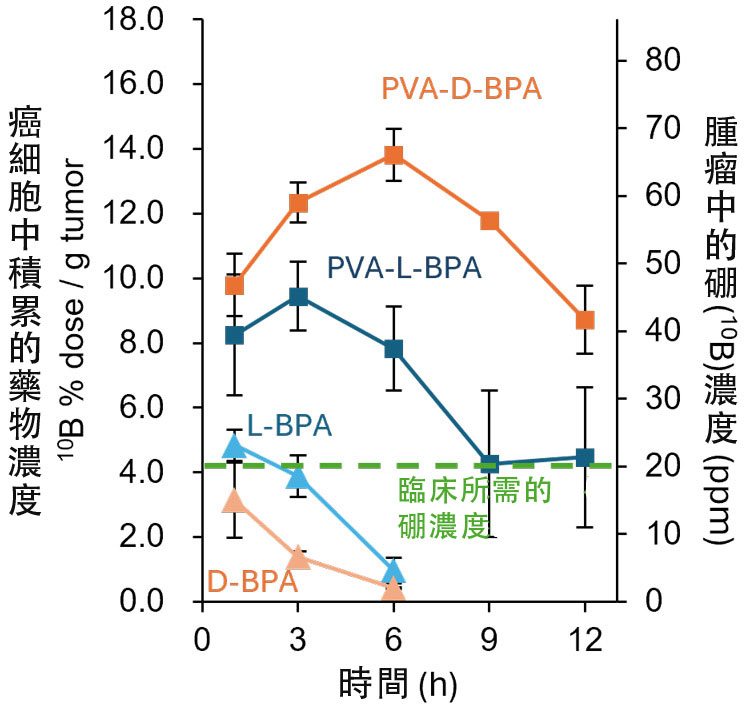
向患有皮下癌的小鼠靜脈注射藥物後,對藥物在癌細胞上的吸收情況進行了檢測。L-BPA和D-BPA與PVA結合時藥物在癌症部位的積聚均有明顯增加,其中PVA與D-BPA組合的藥物表現出更高的濃度和更長的積聚時間(供圖:東京大學野本貴大副教授)
在使用硼中子捕獲療法(BNCT)對小鼠進行實驗時,與目前臨床使用的未加入PVA的L-BPA相比,加入PVA的D-BPA能夠顯著減少癌細胞體積,甚至達到幾乎全部消除的水平。
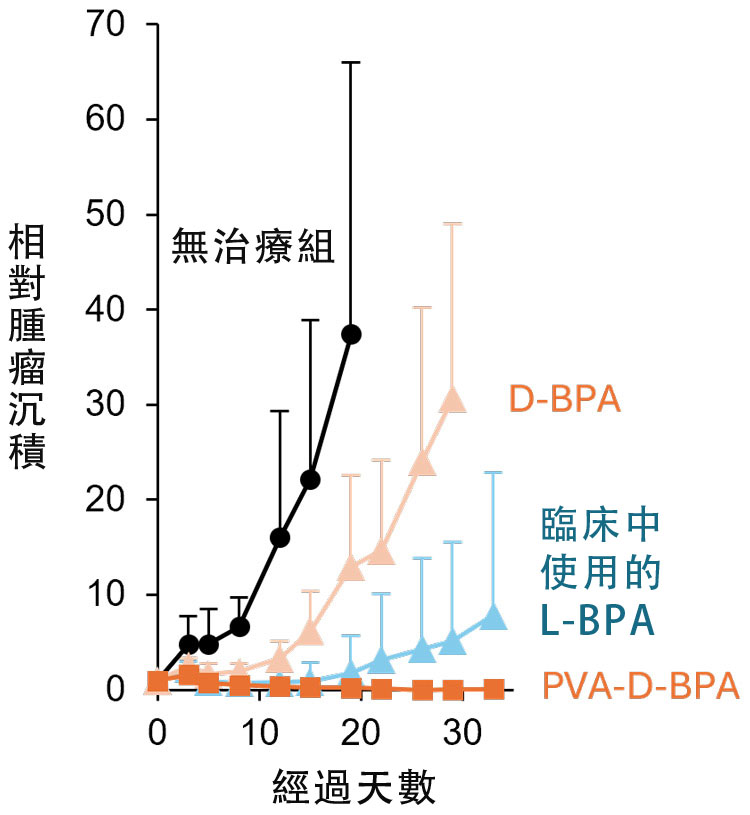
相對體積為1的癌細胞在BNCT治療後的體積變化。臨床上使用的L-BPA和添加PVA的D-BPA藥物,數日內都能減少癌細胞體積。但隨後加入PVA的D-BPA將癌細胞體積進一步縮小到幾乎消失的水平(供圖:東京大學野本貴大副教授)。
野本副教授表示:「通過與PVA組合,D-BPA有望成為治療那些現有藥物效果不足的癌症的有效藥物。」未來計劃通過藥物標準化及更多動物實驗,推動向臨床應用的發展。
本研究由東京大學、京都大學和Stella Pharma公司(大阪市中央區)合作進行,並得到了日本科學技術振興機構(JST)、日本醫療研究開發機構(AMED)、日本學術振興會的科學研究補助金項目及Stella Pharma公司合作研究的經費支持。相關成果於2024年12月3日發表在藥物遞送系統(DDS, Drug Delivery System)專業期刊《Journal of Controlled Release》電子版上。
日文:JST Science Portal 編輯部
中文:JST客觀日本編輯部
【論文資訊】
期刊:Journal of Controlled Release
論文:Poly(vinyl alcohol) potentiating an inert D-amino acid-based drug for boron neutron capture therapy
DOI:10.1016/j.jconrel.2024.11.017