日本東北大學研究生院醫學系研究科Sharmin Naher助教、吉川貴子講師和大隅典子教授等人的研究團隊,與該大學老年醫學研究所、跨學科前緣研究所,國立精神與神經醫療研究中心神經研究所以及臺灣陽明交通大學合作發表研究成果稱,確定了作為運動分子發揮作用的Kif23蛋白是導致小頭症的新的致病分子。研究團隊通過小鼠胎兒期的大腦,考察了小頭症患者中發現的相關基因突變的影響。研究證實,這種致病分子會導致神經幹細胞分裂異常,引發細胞死亡。這一發現有望為未來針對該疾病的基因療法奠定基礎。相關研究成果已發表在國際學術期刊《The EMBO Journal》的2024年12月4日刊上。
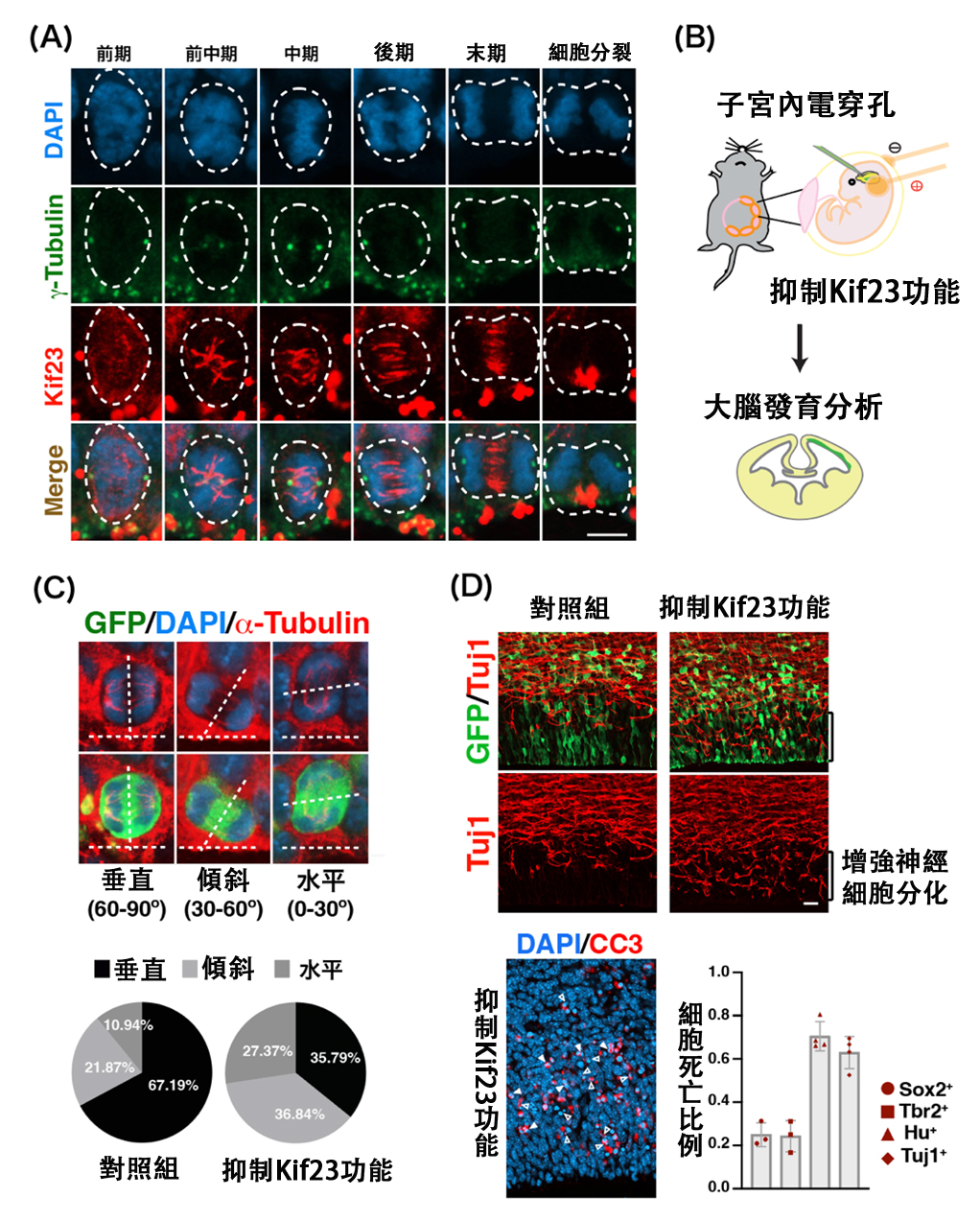
圖1.Kif23在神經幹細胞中的功能(供圖:東北大學)
(A)Kif23在神經幹細胞中的定位。細胞分裂過程包括前期、前中期、中期、後期和末期。在前中期階段,紡錘體開始形成,Kif23開始定位到紡錘體上。Kif23(紅)、γ-tubulin(綠):中心體(細胞進入分裂期時向兩極移動)標記、DAPI(藍):細胞核
(B)利用子宮內電穿孔法對小鼠胎兒大腦進行Kif23功能抑制試驗。
(C)與對照組相比,抑制Kif23的功能可使神經幹細胞的分裂面更水平地傾斜。α-tubulin(紅):形成紡錘體的微管標記
(D)抑制Kif23的功能會導致神經元分化異常和已分化神經元的細胞死亡增加。Tuj1(紅):神經細胞標記、CC3(紅):細胞死亡標記、Sox2(圓形):神經幹細胞標記、Tbr2(方形):中間增殖細胞標記、Hu(三角形):神經細胞標記、Tuj1(菱形):神經細胞標記
小頭症是新生兒頭部尺寸明顯小於平均水平或出生後停止生長的病症,發生概率為數千分之一。患者通常伴隨癲癇、腦癱、學習障礙等問題。病因包括基因異常、子宮內感染、有毒化學物質的暴露以及胎兒期嚴重營養不良。目前尚無有效的治療方法。
神經幹細胞會自我增殖並分化成神經細胞,而神經細胞不再具有增殖能力。大腦發育始於胎兒期,由神經幹細胞通過分裂和分化構建。由於神經細胞的分化在胎兒早期即完成,所以即使已知小頭症的病因主要發生在胚胎發育早期階段,但許多細節仍不清楚。
此前已有研究報告顯示,與小頭症相關的突變基因多與細胞分裂有關。另一方面,雖然KIF23基因被指出與小頭症有關,但其具體機制尚不明確。
KIF23所編碼的蛋白質已被確認是一種通過微管運輸物質的運動分子(即動力蛋白家族成員之一)。
研究團隊用小鼠胎腦模型觀察Kif23蛋白在神經幹細胞分裂過程中的分佈情況。結果發現,其局部定位於紡錘體區域。
為了研究其該蛋白質對活體小鼠胎兒大腦發育的影響,研究團隊通過子宮內電穿孔和RNA干擾技術抑制了Kif23的表達。
結果顯示,神經細胞的分化程度較正常情況增加了20%至30%,並且一過性神經細胞數量增加。
此外,在抑制該蛋白質功能的胎鼠體內,僅神經細胞發生細胞死亡,表明可能是由於細胞分裂異常導致的。
為了驗證在人類小頭症患者中觀察到的Kif23基因突變是否為致病因素,團隊將人類KIF23突變基因導入到Kif23功能抑制的小鼠模型中,誘導了強製表達。
結果顯示,確認了神經細胞分化的亢進,並證實這種亢進可以通過導入人類正常型KIF23基因得到抑制。而導入人類小頭症變異型KIF23基因時,神經細胞分化的亢進未能得到充分抑制。
吉川講師表示,「目前還沒有治癒小頭症的方法,但未來如果基因療法進一步發展,KIF23有望作為小頭症治療的靶點發揮作用。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:The EMBO Journal
論文:Kinesin-like motor protein KIF23 maintains neural stem and progenitor cell pools in the developing cortex
DOI:10.1038/s44318-024-00327-7