愛知醫科大學病理學講座豬子誠人講師主導的研究團隊發表研究成果稱,成功開發出了可在體外長期增殖人類上皮組織前驅物的未成熟基底細胞,並能在短期內促熟(分化)的新技術。通過該技術對比分化前後的狀態,發現未成熟的正常基底細胞與癌細胞之間存在共性。該成果有望應用於再生醫療、癌症研究等多項醫療開發領域。相關研究成果已發表在國際學術期刊《Scientific Reports》4月9日刊上。
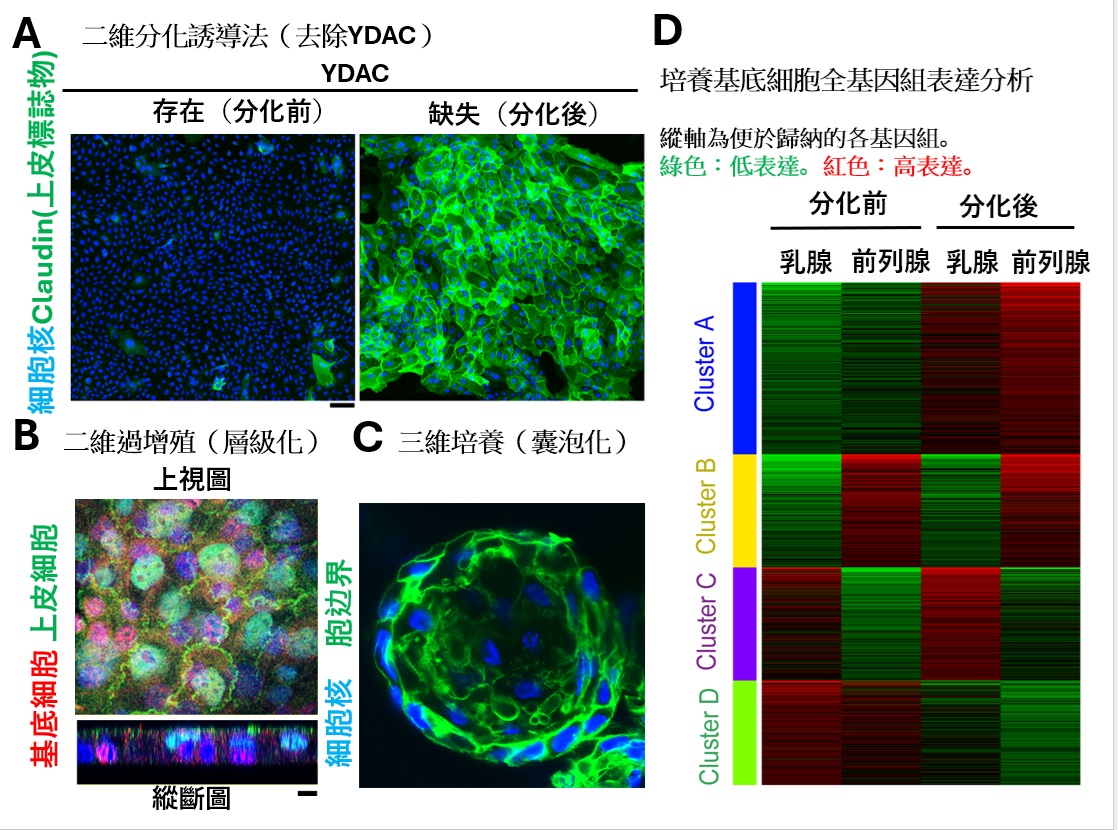
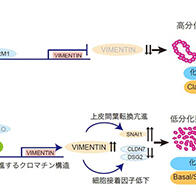
圖1:新開發的正常乳腺基底細胞的體外分化誘導法(供圖:愛知醫科大學豬子誠人)
上皮組織是保護機體免受外界侵害的重要屏障,其屏障功能由被稱為「緊密連接(tight junction)」的分化上皮特有的細胞間連接結構維持。其主要蛋白質「克勞丁(Claudin)」於1998年由京都大學首先報告,並證實其對上皮屏障的形成至關重要。但是此前難以在體外實現未成熟上皮的可控分化,其成熟過程機制一直不明確。
對此,研究團隊此次以初代培養常用的培養基F-medium為基礎,新設計了添加名為YDAC的四種藥物組合的培養基。通過該培養基,成功實現了人類乳腺基底細胞在體外的長期增殖。進一步研究發現,該狀態下更換為去除化合物的培養基後,可在保持平坦二維狀態的同時,短時間內高效分化為上皮細胞。YDAC是ROCK抑制劑Y-27632、SMAD抑制劑DMH1與A-83-01、Wnt活化劑CHIR99021的混合物。
此外,研究團隊確認,當基底細胞在二維環境中過度增殖時,會形成與生物組織相似的層狀結構。同時也證實,通過使用現有的類器官培養法進行培養,這些細胞能夠分化為更接近生物體內的三維囊泡狀結構體。
對分化前後的基因表現進行分析後發現,分化後乳腺上皮特有的基因群表達量出現上升。
研究還明確,分化前轉錄因子EGR1表達活躍,而分化後ELF3的表達則顯著增強。
因此,研究團隊進行了分別敲除這兩種轉錄因子的實驗,結果顯示,敲除未成熟基底細胞中的EGR1後,Claudin開始表達,而敲除成熟上皮細胞中的ELF3後,Claudin的定位則受到抑制。這一結果表明,這兩種轉錄因子分別參與了Claudin的表達抑制和定位。
已知EGR1的表達與ELF3的缺失與癌症的上皮間質轉化(EMT:參與浸潤、轉移等過程)有關,這一發現揭示了癌細胞與正常基底細胞之間的共通點。該結果在乳腺組織及類器官培養法中也得到了關聯性驗證。
豬子講師表示:「自從在醫學院接觸細胞生物學以來,我一直希望能建立一個貼近臨床的細胞解析系統。iPS和類器官技術的發展為此提供了助力,此次我們開發出了一種簡單明瞭且具有解析能力的研究方法體系。目前我們正在致力於將其應用於癌症培養研究,並且已經取得了一定的成果。如果有對共同研究感興趣的人士,歡迎訪問 researchmap。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Scientific Reports
論文:Long-term expansion of basal cells and the novel differentiation methods identify mechanisms for switching Claudin expression in normal epithelia
URL:https://www.nature.com/articles/s41598-025-95463-3