日本大阪大學微生物病研究所的小瀧將裕助教、龝枝佑紀助教、石谷太教授、小林剛教授等人組成的研究團隊,與和歌山縣立醫科大學、地方獨立行政法人大阪健康安全基盤研究所共同宣佈,利用斑馬魚成功人工合成了人類諾如病毒。該成果是通過使用斑馬魚胚胎(魚卵)實現的。研究還確認,人工合成的諾如病毒可以進行連續傳代,並且能夠自由引入突變。這是人類首次在魚類胚胎中人工合成人類致病病毒。該成果有望成為闡明諾如病毒的感染機制以及推進疫苗開發的重要基礎。相關研究成果已發表在美國國家科學院院刊《PNAS》的12月4日刊上。
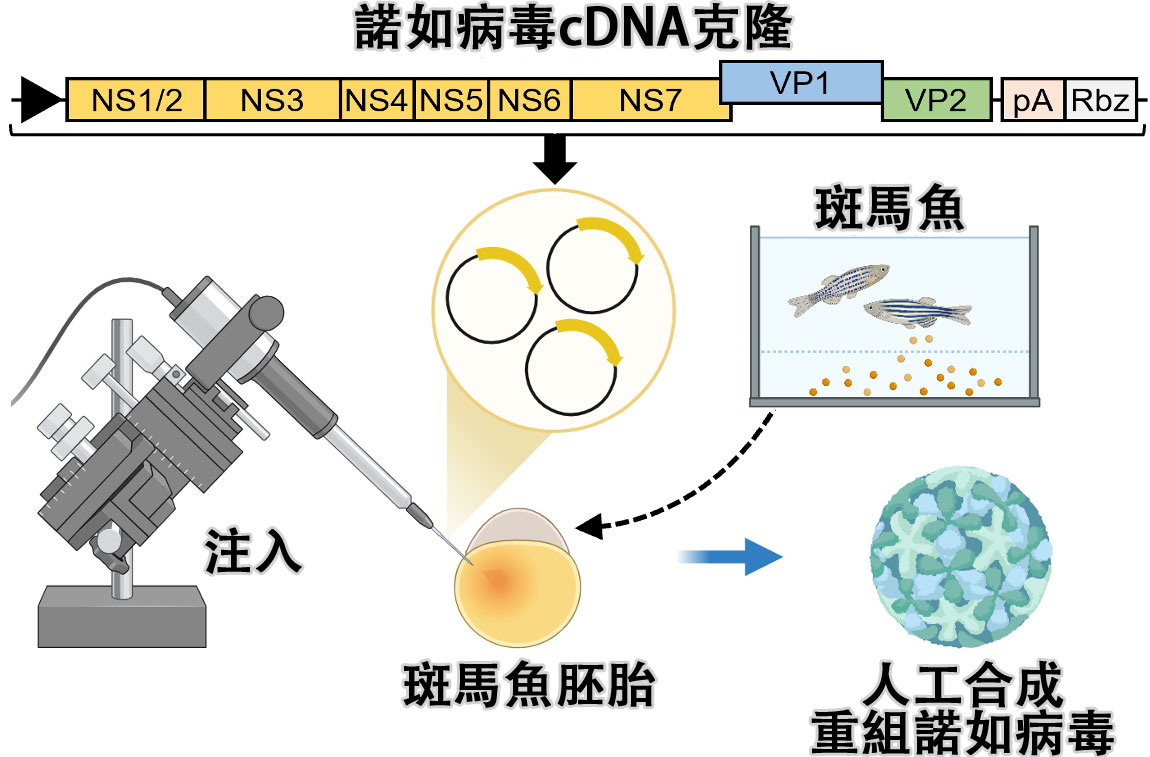
圖1 利用斑馬魚胚胎的諾如病毒人工合成(供圖:大阪大學)
諾如病毒是一種感染力極強的RNA病毒,可引起腹瀉、嘔吐等症狀,是食物中毒的重要致病原因之一。從醫療費用負擔的角度來看,加強相關的公共衛生防控措施已成為當務之急。諾如病毒具有多種基因群和基因型,全球每年約有7億人感染,其中以發展中國家為主每年約有20萬人因此死亡。
然而,由於諾如病毒的培養體系和人工合成方法尚未建立,相關研究一直未能取得實質性進展。
一般而言,病毒研究通常使用培養細胞來實現病毒增殖,但諾如病毒無法在培養細胞中增殖。腸道類器官是目前唯一能夠支持諾如病毒增殖的體系,但其成本高昂,且數代後便會停止增殖。約在10年前,已有研究稱諾如病毒可在斑馬魚胚胎中增殖,但該體系是否具備可連續傳代的能力、以及病毒感染性是否能夠維持等關鍵問題仍不明確,因此斑馬魚胚胎能否作為穩定的研究基礎平台一直存疑。
RNA病毒的人工合成技術是一種將來源於病毒基因組的核酸導入培養細胞內,從而合成具有感染性的重組病毒的技術,在病毒研究領域已得到廣泛應用。
此前,該研究團隊已開發出包括輪狀病毒在內的多種RNA病毒人工合成技術。
因此,此次研究團隊首先將來源於3種諾如病毒株基因型(GⅡ-4型、GⅡ-2型、GⅡ-17型)的cDNA,通過顯微注射法注入斑馬魚胚胎中,驗證其是否能夠實現增殖。
結果顯示,所有病毒株均能高效實現病毒增殖。其中,GⅡ-17型還被發現會在孵化後的幼體中引發水腫。此外,將孵化幼體壓碎後獲得的病毒再次用於斑馬魚胚胎的連續傳代時,確認到病毒能夠持續增殖,且至少可完成5次傳代。
隨後,研究團隊進一步探討了將培養細胞與斑馬魚胚胎相結合的人工合成方法。
將含有GⅡ-17型諾如病毒cDNA的質體(cDNA選殖)導入培養細胞中,然後對生成的病毒粒子進行濃縮,並通過顯微注射注入斑馬魚胚胎,確認可製備重組病毒。此外,所獲得的重組諾如病毒同樣可以進行連續傳代,並且已證實其能夠感染腸道類器官。
此外,研究團隊還成功通過導入外源基因,構建了發光型病毒,並確認該體系可用於評估病毒的增殖能力以及抗病毒藥物的效果。
另外,研究團隊還進一步探索了更高效的合成方案。研究結果表明,無需經過培養細胞步驟,而是直接將諾如病毒cDNA選殖通過顯微注射注入斑馬魚胚胎,同樣能夠高效製備重組病毒。
研究團隊還成功製備了在人類中佔主導流行地位的GⅡ-4型諾如病毒。病毒在注入後2天內即開始增殖,並已確認具備可連續傳代的能力。
小林教授表示:「此次成功利用斑馬魚實現諾如病毒的人工合成,不僅在小型魚類研究領域提出了人工構建病毒這一新的應用方向。此外,該技術還有望為闡明諾如病毒的增殖機制,以及為疫苗和治療藥物的開發作出了廣泛貢獻。通過推進諾如病毒治療藥物和疫苗的研發,我們希望進一步推進相關研究,在未來能夠為人們的健康與福祉作出貢獻。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Proceedings of the National Academy of Sciences of the United States of America (PNAS)
論文:Recovery of Infectious Recombinant Human Norovirus Using Zebrafish Embryos
DOI:10.1073/pnas.2526726122