嵌合抗原受體T細胞療法(CAR-T細胞療法)在白血病、惡性淋巴瘤及多發性骨髓瘤等血液癌領域效果尤其顯著,針對各類實體癌,以臨床應用為目標的研發工作也在積極推進之中。然而,在部分血液癌患者得以治癒的同時,也有不少復發案例。
京都大學研究生院醫學研究科發育兒科學的瀧田順子教授、平松英文講師(現任近畿大學醫學部兒科講師)、加藤格講師、三上貴司特定研究員(現任該研究科附屬癌症免疫綜合研究中心特定助教)、該研究科血液內科學的高折晃史教授、大阪大學感染症綜合教育研究基地感染症與生體防禦研究部門的James Wing教授等人組成的研究團隊發現,在針對難治性前驅物B細胞急性淋巴細胞白血病(BCP-ALL)的復發患者使用CD19 CAR-T細胞療法時,細胞製劑內特定細胞——4MD CAR-T細胞較多時,治療效果較好。這種CAR-T細胞的免疫抑制性腺苷產生量較少,具備可長期存活的記憶T細胞性質,因此被認為能夠有效清除癌細胞。相關研究成果已發表在期刊《Cell Reports Medicine》上。
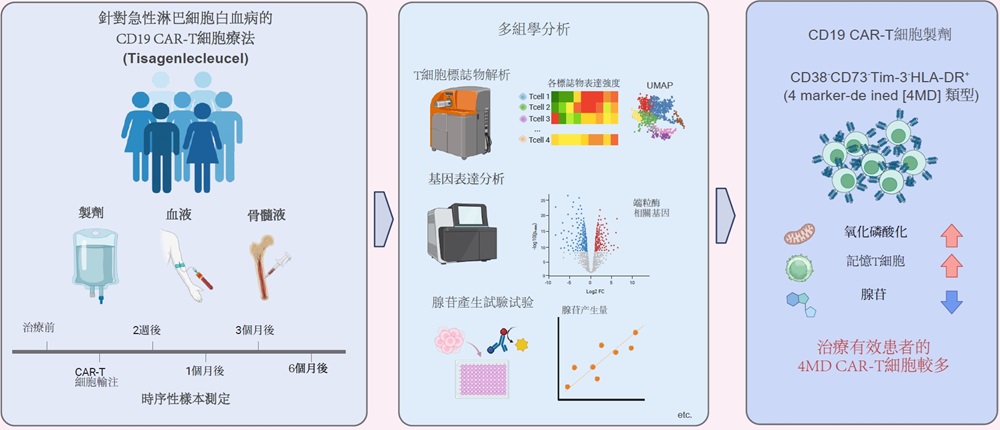
圖1 接受CD19 CAR-T細胞(tisagenlecleucel)治療的BCP-ALL患者多組學分析(使用 BioRender 繪製。作者:京都大學 三上貴司,使用許可:CC BY 4.0。)
研究團隊著眼於CD19 CAR-T細胞療法療效好與療效不好的患者之間有何差異,開展了可預測治療效果的生物標誌物探索研究。研究以2019年至2023年間在京都大學醫學部附屬醫院接受給藥治療的BCP-ALL患者(兒童16例、年輕成人3例)為對象,在治療前後的時段內,時序性地採集CAR-T細胞製劑、血液、骨髓液並進行分析。研究結合質譜流式細胞術(CyTOF)、小滴式數字PCR、基因表現分析、細胞檢測等多種技術手段展開,對CAR-T細胞進行了多向度的評估。
運用CyTOF的細胞標誌物分析發現,當CAR-T細胞製劑中,具備CD38陰性、CD73陰性、Tim3陰性、HLA-DR陽性特徵的T細胞(4 marker defined: 4MD)較多時,治療效果較好且不易復發。在4MD的標誌物中,CD38與CD73參與細胞外腺苷的產生,而腺苷已知具有免疫抑制作用。T細胞的檢測實際證實了4MD CAR-T細胞腺苷產生較少。此外,基因表現分析揭示,4MD CAR-T細胞的氧化磷酸化及粒線體活性較高,具備記憶T細胞的特徵,易於長期維持免疫活性。研究認為,4MD CAR-T細胞正是憑藉這些特性,可有效清除白血病的癌細胞,助力提升治愈率。
該結果也在另一項既往研究的單細胞RNA-seq數據中得到驗證:根據4MD標誌物特徵將患者分為兩組後,證實接受4MD標誌物高佔比CAR-T細胞製劑給藥的患者復發率更低。
4MD標誌物與T細胞的活化、耗竭等免疫學性質相關,可能同樣適用於靶向其他抗原或癌症的CAR-T細胞。今後,為實現這類CAR-T細胞的高效製備,研究團隊表示將繼續研究從患者體內採集的T細胞是否天然具備相關質,同時探討基因導入與培養條件,致力於開發出更高效的CAR-T細胞療法。
三上特定助教表示:「為了讓CAR-T細胞療法能成為更多患者的希望,我們將繼續從腫瘤免疫學的視角出發,以革新新的治療方法為目標,不懈努力。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Cell Reports Medicine
論文:CAR-T cells with the CD38⁻CD73⁻Tim-3⁻HLA-DR⁺ phenotype predict the efficacy of tisagenlecleucel as a treatment for B cell precursor ALL
DOI:doi.org/10.1016/j.xcrm.2025.102576