日本大阪大學研究生院工學研究科的筒井裕哉博士生(研究當時)、工學部應用自然科學科的大四學生志賀心、小西彬仁助教、安田誠教授等人組成的研究團隊,全新開發併合成出了以14族元素(碳族元素)為中心、具有特殊籠狀結構的烯丙基化試劑(烯丙基雜氮三環化合物),並在全球首次證實可通過與既往不同的路徑來實現反應控制。相關研究成果已發表在《Nature Communications》上。
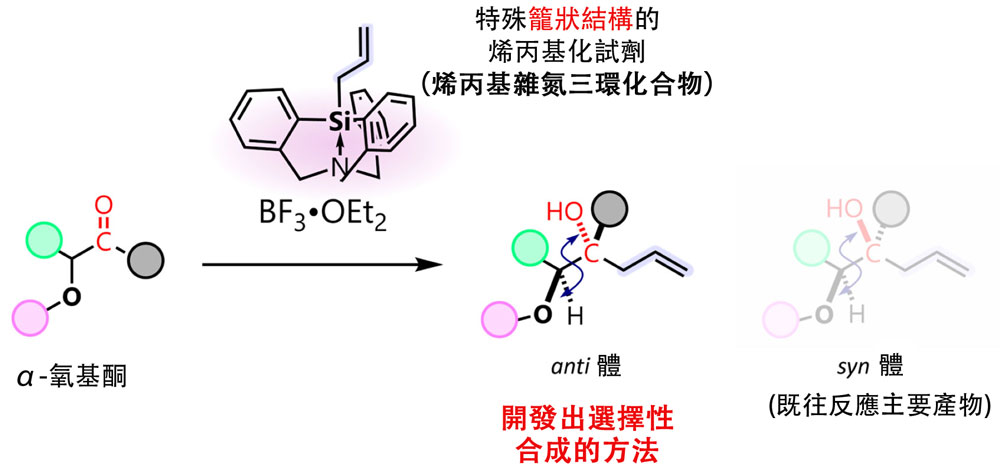
圖1.利用籠狀結構烯丙基化試劑實現具有全新空間排列的烯丙基化反應(供圖:大阪大學)
在有機合成化學中,羰基化合物親核加成反應中的立體選擇性控制,是決定分子功能的關鍵課題。尤其是在α位含有氧原子的α-氧基羰基化合物,作為天然產物合成與藥物合成中的重要構成要素而被廣泛應用。
此前,在α-氧基羰基化合物的烯丙基化反應中,由氧原子強螯合配位金屬的螯合控制佔據主導地位,反應被認為只能生成單一方向的空間排列(syn體)。因此,通過不依賴金屬配位的路徑(非螯合路徑),選擇性地獲得相反空間排列(anti體)顯得極其困難,是長期以來都未能解決的難題。
此次,研究團隊全新開發併合成了以碳族元素(矽、鍺、錫)為中心的烯丙基雜氮三環化合物,並證實使用該試劑可實現不依賴金屬配位的非螯模具組裝反應控制。
這類烯丙基雜氮三環化合物,憑藉分子內形成的特殊籠狀結構,具備高親核性,同時具有能抑制金屬本身路易斯酸性的特性。
此外,通過實驗與理論計算相結合的分析,研究團隊闡明瞭該試劑經與既往螯合控制不同的反應路徑,可使α-氧基酮的烯丙基化反應以高anti選擇性進行。該方法適用於多種受質,能夠以高產率和高選擇性製備出既往方法難以實現的空間排列的產物。
本研究實現了此前被認為無法達成的α-氧基羰基化合物的非螯模具組裝立體控制。這是拓展有機合成立體選擇性控制基礎概念的重要成果。尤其在立體結構直接決定生理活性的藥物與生理活性物質的合成中,該方法有望成為能夠精確製備與既往方法不同的立體異構物的全新合成策略。同時,作為藥物研發與高性能分子設計的基礎技術,預計未來將擁有廣闊的應用前景。
安田教授表示:「在有機合成化學中,碳碳鍵形成反應是最重要的基礎技術,在此過程中,需要控制分子之間以何種空間排列進行結合。對於α-氧代羰基化合物,雖然已經確立了通過使用金屬的螯合控制來選擇性獲得單一產物的方法,但獲得相反方向連接的產物此前一直被認為無法實現。在以非螯合控制為目標、歷經多年反復試錯的過程中,我們遇到了諸如反應試劑不穩定等諸多難題,而此次發現的籠狀結構試劑,終於讓我們攻克了這一長期難題。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Nature Communications
論文:Non-Chelation Control in Allylations of α-Oxy Ketones Using Group-14 Allylatranes
DOI:doi.org/10.1038/s41467-026-69732-2