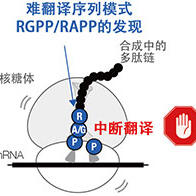
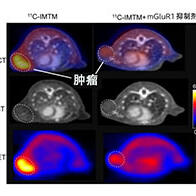
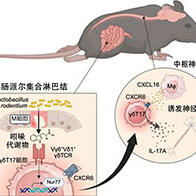
國立研究開發法人日本醫療研究開發機構(AMED)正在實施一項啟動與2024年,為期5年的「智慧生物製藥研究支援事業」項目。為推動日本自主研發出創新型生物藥品,該項目以「升級至臨床試驗」為目標。目前共有19個下屬項目正在推進,我們將分多期介紹這些具備開發潛力的「生物藥品原石」。

圖1 東京大學研究生院藥學系研究科的金井求教授(供圖:東京大學)
我們基於被譽為自然界最強的鏈黴親和素與生物素的親和性,開發出了兼具低免疫原性與抗體內生物素干擾特性的藥物遞送系統——Cupid-Psyche系統。Cupid-Psyche系統由鏈黴親和素修飾蛋白Cupid與生物素修飾低分子Psyche構成,僅需將二者簡單混合即可生成Cupid-Psyche以1:2比例結合的、完全均質的複合製劑。構建該平台時,首先通過蛋白質工程技術改造存在於鏈黴親和素的生物素結合口袋中的特定氨基酸殘基,使其與生物素的結合強度降至檢測限以下(Cupid)。由此構建出不受生物體內以輔酶存在的生物素(維生素B7)影響的系統。
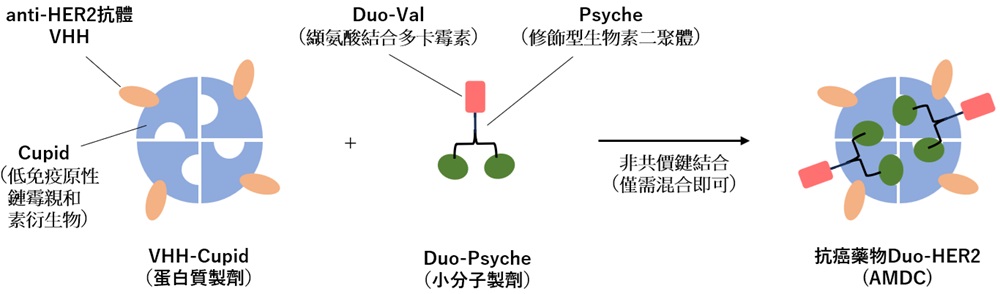
圖2:AMDC概念示意圖(以抗HER2-Cupid與Duo-Psyche為模型展示)(供圖:東京大學)
其次,通過有機合成化學方法改造生物素結構使其與修飾蛋白的結合口袋結合,並進一步將其二聚合化以實現二價結合,從而獲得強效結合能力(Psyche)。如果將融合抗癌原抗體的Cupid與結合抗癌藥物的Psyche複合,便可實現抗癌藥物對癌細胞的選擇性遞送。Cupid-Psyche系統作為一個強大平台,可將同位素、光敏劑等各類酬載輸送至不同癌細胞靶點,已被證實能為多樣化抗癌策略提供有效基礎。
「智慧生物製藥研究支援事業」中採用的酬載多卡黴素(Duo)是一種具有極強抗腫瘤活性的天然來源的抗生素,在皮摩爾級別的極低濃度下即可顯示細胞毒性。Duo通過結合DNA雙螺旋的小溝,並使DNA烷基化阻斷複製與轉錄,最終誘導細胞死亡。因其強烈的細胞殺傷能力,若直接作為常規抗癌藥物使用,將對正常細胞產生過度毒性並引發嚴重副作用。另一方面,若採用僅向靶向癌細胞遞送Duo的藥物遞送系統,則有望作為癌症治療藥物發揮卓越療效。
基於上述背景,我們正致力於利用具有針對HER2(伴隨復發轉移的實體進展期癌症關鍵抗原)的重鏈抗體(VHH)人工抗體模擬物VHH-Cupid,與僅需極少量分子即可殺傷癌細胞的Duo結合而成的Duo-Psyche,開發Duo結合的抗HER2抗體模擬物複合製劑,即Duo-HER2(上圖)。現有成果表明,Duo-Psyche的大規模穩定供應已成為可能。小鼠實驗證實,Duo-HER2可在不產生副作用的情況下根治癌症,且展現出相較現有藥物的顯著優勢。今後,研究團隊將進一步加速研究,致力於向人類臨床階段的推進,力求盡快為飽受病痛折磨的患者及其家屬提供優秀的抗癌藥物。
原文:《科學新聞》
翻譯:JST客觀日本編輯部