名古屋大學學術研究與產學官合作推進本部的浜口知成特任講師、大野欽司名譽教授(現任名古屋學藝大學教授)等組成的研究團隊指出難以治療的慢性特發性便秘是由兩種腸道細菌互利共生引發的,並提出了新概念「細菌性便秘」,有望為治療方法的開發提供方向。相關成果已發表在《Gut Microbes》的2月18日刊上。
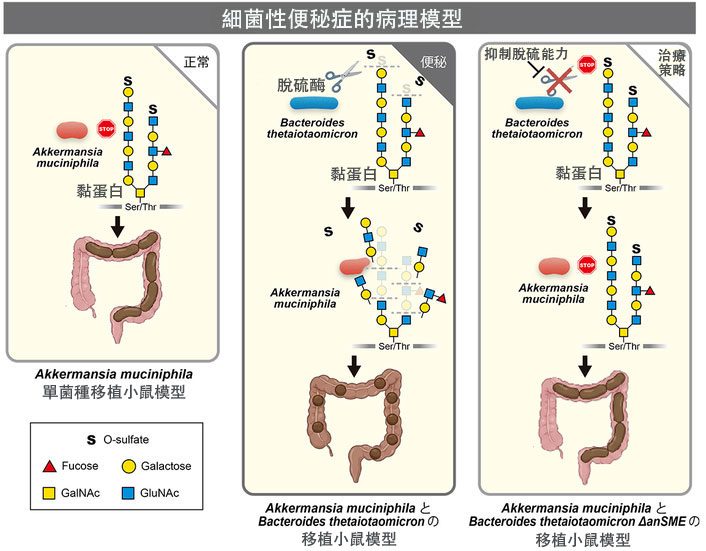
圖1 細菌性便秘症的病理模型(供圖:名古屋大學)
便秘是以排便次數減少、糞便堅硬為特徵的常見消化系統疾病,其病因此前一直被認為是「腸道蠕動功能下降」。然而,對於與腸道蠕動無關、病因不明的慢性特發性便秘症(CIC)以及巴金森氏症(PD)伴隨發生的便秘,其發病機製此前一直不明確。CIC及PD相關便秘難以通過輕瀉劑或刺激性藥物得到改善。
因此,此次研究團隊關注了可保持糞便水分、使腸道內潤滑的成分「腸道黏液」,驗證了腸道黏液被腸道細菌分解而引發便秘的可能性。
腸道黏液以聚合物醣蛋白黏蛋白為主要成分,黏蛋白具有高保濕性,覆蓋於腸道內側,在保護腸壁免受細菌侵害的同時,還承擔著使排便順暢的潤滑劑作用。
首先,為確定致病腸道細菌,研究團隊對從全國收集的147名健康者、231名巴金森氏症患者、54名慢性特發性便秘患者的糞便進行了16S解析及qPCR解析。結果發現,患者糞便中B.thetaiotaomicron 和A.muciniphila 兩種細菌出現異常增殖。
接下來,為研究這些腸道細菌的功能,研究團隊開展了將細菌移植給無菌小鼠的實驗。結果顯示,單獨移植任一細菌均不會引發便秘,而同時移植兩種細菌則會出現糞便變硬(重量降低)、排便次數減少的便秘症狀。這表明兩種細菌互利共生引發了便秘。而移植8種腸道細菌的無菌小鼠(對照組)則未出現便秘。
此外,通過腸壁通滲透性實驗證實,在兩種細菌共存的情況下,腸道屏障功能受到抑制,出現腸漏(腸道通滲透性增加)。
已有報導稱,B.thetaiotaomicron 具有脫去硫酸基團的功能,而A.muciniphila 不具備該功能,但能夠特異性分解黏蛋白。基於此,研究團隊驗證了B.thetaiotaomicron 脫去保護黏蛋白的硫酸基團,再由A.muciniphila 對其進行分解的可能性。
研究團隊製備了失去腸道黏膜去硫化功能(缺失anSME酶基因)的B.thetaiotaomicron 菌株,並將其與A.muciniphila 共同定植於無菌小鼠體內,結果確認便秘得到緩解。研究還證實,將該菌株與A.muciniphila 同時移植給小鼠後,小鼠的糞便團塊數量及糞便重量均有所增加,便秘受到抑制。
浜口特任講師表示:「我們認為,細菌性便秘症是由於細菌本身分解黏蛋白黏液的能力異常升高而發病。作為治療思路,目前還只是提案階段,但可以考慮開發抑制關鍵開鎖酶作用的藥物,或使用不感染人體、僅特異性感染並清除細菌的噬菌體進行治療。今後我們將致力於開發以細菌而非以人體為靶點、副作用更少的根本性治療方法。」
大野名譽教授表示:「本次我們提出‘細菌性便秘’並闡明其機制,有望實現靶向性更高的治療。增強酶活性的藥物開發難度較高,相比之下,抑制酶活性的藥物雖然相關研究較少,但我們認為其實現可行性相對更高。」
注 無菌小鼠:
指在體內及體表完全不存在任何微生物的狀態下飼養的小鼠。它們在特殊隔離裝置(Isolator)中,被餵食完全滅菌的水和飼料進行培育。本研究中,通過向這些無菌小鼠僅投予特定細菌使其定植,製備了悉生小鼠。另外,開展本研究的實驗室首任教授宮川正澄於1954年在世界上首次成功培育出無菌豚鼠。當年宮川教授開創的「無菌動物」研究技術歷經數十年,至今仍被應用於醫學生物學研究。本研究與發展了無菌動物實驗的實中研(CIEM)共同進行,並接受了技術指導。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Gut microbes
論文:Bacterial constipation: Mucin-degrading intestinal commensal
bacteria cause constipation
DOI:10.1080/19490976.2025.2596809