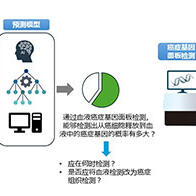
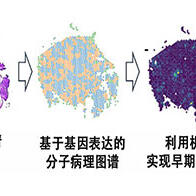
國立研究開發法人日本醫療研究開發機構(AMED)正在實施一項啟動與2024年,為期5年的「智慧生物製藥研究支援事業」項目。為推動日本自主研發出創新型生物藥品,該項目以「升級至臨床試驗」為目標。目前共有19個下屬項目正在推進,我們將分多期介紹這些具備開發潛力的「生物藥品原石」。

圖1 日本東北大學研究生院醫學系研究科加藤幸成教授(供圖:東北大學)
近年來,抗體藥物在生物藥品銷售額中的佔比攀升至極高水平。除常規的免疫球蛋白G(IgG)外,雙特異性抗體(BsAb)、小分子化抗體(scFv及奈米抗體)等各類結構形式的抗體相繼被開發成功,抗體在抗體藥物偶聯物(ADC)、T細胞誘導療法(TCE)、嵌合抗原受體T細胞(CAR-T)療法等各種使用抗體的模態中的應用日益活躍。尤其是BsAb與ADC組合(BsAb-ADC)的臨床應用愈發盛行,海外癌症相關學術會議中,BsAb-ADC臨床試驗的講題隨處可見。但目前對於何種靶點分子組合更優、何種特性的抗體更好等問題尚未得到明確答案。此外,針對實體瘤的CAR-T療法,儘管眾多製藥企業及學術界研究人員均在攻關,但全球範圍內至今尚無一款產品上市。綜上不難看出,該領域仍存在諸多亟需解決的問題。日本東北大學並未聚焦競爭日趨激烈的模態開發,而是專注深耕於最基礎的單源抗體研發。在生物藥品研發領域,單源抗體開發或許是最低調樸實的工作,但每日都能體會到抗體製備的博大精深。

圖1 流式細胞分析技術(供圖:東北大學)
迄今為止,東北大學始終聚焦於癌細胞特異性抗體(CasMabR)的研發。無論抗體應用於何種模態,對正常組織的毒性始終令人擔憂,但僅在癌細胞中高表達的分子十分有限,理想的靶點分子已經枯竭。由此我們認為,即便相關分子在正常細胞中也高表達,只要能製備出無副作用的抗體藥物,難治性癌症治療方法的開發就能一舉取得進展。基於這一思路,在AMED既往項目——「創新性生物藥品創製基礎技術開發事業」及「尖端生物新藥創製基礎技術開發事業」實施的10年間,我們為解決這一問題開展了創新性技術研發,累計向企業輸出了56項抗體種子。「智慧生物製藥研究支援事業」啟動至今尚未滿2年,我們已將2種針對膜蛋白的CasMab輸出給了企業。

圖2 CO₂培養箱(供圖:東北大學)
即便嘗試檢測正常細胞與癌細胞中表達的蛋白差異,也幾乎無法發現二者在氨基酸突變或糖鏈結構上的區別,但我們已能夠通過自主開發的方法,獲得可特異性識別癌細胞中可見的細微結構變化的CasMab。針對乳腺癌、胃癌中高表達的HER2的CasMab已完成了向企業的技術輸出,相應CAR-T療法已於2024年1月在美國啟動臨床試驗,截至目前完全沒有收到毒性相關報告。未來,東北大學仍將以快速、高精度製備針對難治性癌症的CasMab為目標,持續推進研發工作。如前所述,抗體製備是一項非常低調樸實的工作,但研究室配備了大量檢測設備(流式細胞分析技術:目前14臺),正進行高通量抗體製備;同時使用大量培養設備(CO2培養箱:目前32臺),實施大規模的抗體生產。我們將通過這樣低調樸實的工作,持續向製藥企業進行輸出。
我們認為,學術界專注於開發獨具原創性的藥物種子,成果移交製藥企業後,由製藥企業主導負責臨床試驗,這才是正確的職責分工。從學術界到企業的種子輸出固然是重要課題,但絕非最終目標。將藥物種子推進至臨床試驗階段、送到患者身邊,拯救沒有治療方法、飽受病痛煎熬的患者才是重要的。未來我們也將接連不斷地開發CasMab,為攻克難治性癌症砥礪前行。
原文:《科學新聞》
翻譯:JST客觀日本編輯部