在當前的癌症治療領域,採用小分子化合物或抗體藥物的分子靶向藥物,因對特定靶標因子具有高親和性,已成為治療的主流手段。但這些傳統療法大半以「單一基因(或蛋白質)」為靶點,在多條信號轉導電的路失調、且由異質性細胞群形成的癌症中,無法獲得充分治療效果的情況屢有發生。

圖1 廣島大學研究生院醫系科學研究科高橋陵宇副教授(供圖:廣島大學)
此外,傳統癌症治療還存在兩大壁壘。第一,存在大量基因雖與癌症的惡性進展及轉移密切相關,但由於受蛋白質結構問題(Undruggable target)的限制,現有分子靶向藥物難以對其進行調控;第二,對單一分子的抑制會引發代償性信號激活,最終導致腫瘤獲得「抗藥性」,這會嚴重惡化患者的預後。社會各界迫切期待創製出可攻克上述難題的新型治療模式。
為打破這一現狀,我們將目光投向了作為新一代抗癌藥物的核酸藥物,尤其是非翻譯型RNA的一種——微RNA(microRNA:miRNA)。miRNA具有現有藥物不具備的的「多分子靶向能力」,能以單個分子對帶有互補序列的多個靶傳訊RNA(mRNA)的表達進行廣譜性抑制。
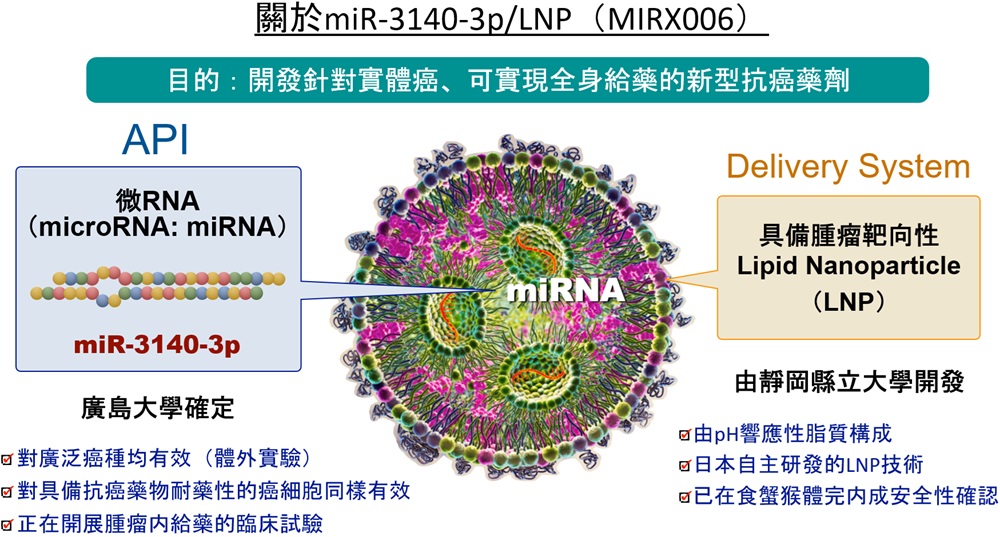
圖2 miR-3140-3p/LNP製劑(MIRX006)的開發(供圖:廣島大學)
研究團隊在既往研究中已獨立發現特定miRNA「miR-3140-3p」具有極強的抗腫瘤效果。對於癌症這類同時存在多種基因異常或複雜信號調控紊亂的疾病,可全面靶向多條信號通路的miR-3140-3p,有望成為極有效的新藥研發種子。本研究將miR-3140-3p作為核酸藥物的主要成分,旨在實現傳統分子靶向藥物無法達成的「杜絕抗藥性的癌症治療」。
核酸藥物實現實用化的最大壁壘,在於向靶組織的遞送效率、生物體內的穩定性,以及避免對正常組織產生副作用。本研究為最大限度發揮miR-3140-3p的潛能,正同步開發高度腫瘤選擇性遞送系統。
具體利用了實體瘤周圍微環境相較於正常組織呈「酸性(低pH)」的生理學特徵。本研究設計了以僅在特定酸性條件下可被細胞攝取的「pH 響應性脂質」為材料的脂質奈米顆粒(LNP),藉此構建了一套可兼顧保持血液中穩定存在、到達腫瘤組織時響應酸性環境並高效釋放導入miRNA的遞送系統。本技術的目標是,實現即便全身給藥也能將副作用降至最低、同時具備極高治療效果的藥物遞送。
本研究將具備強效抗腫瘤活性的「miR-3140-3p」與「腫瘤選擇性遞送技術」相融合,推進了全身給藥型新型核酸候選藥物「MIRX006」的開發。研發工作將圍繞以下兩大主軸開展:第一是生物學評價,旨在通過跨癌種的有效性驗證、詳細作用機制的闡明,以及安全性試驗法,積累非臨床數據;第二是物性方面的相關研究與生產開發,旨在實現脂質奈米顆粒優化,並確立面向藥品開發的生產工藝。
通過深化這兩大方向的研究,將切實推動MIRX006實現「臨床進階(進入臨床試驗)」。本研究的完成,不僅將會為難治性癌症患者提供新的治療選擇,也將為日本核酸藥物研發技術平台的確立做出重大貢獻。
原文:《科學新聞》
翻譯:JST客觀日本編輯部