日本國立研究開發法人理化學研究所生命醫科學研究中心的秦咸陽高級研究員、鈴木治和團隊總監,以及千葉縣癌症中心研究所、岐阜大學、東京慈惠會醫科大學的研究團隊聯合發表研究成果稱,發現轉錄因子之一的MYCN蛋白會促進原發性肝癌的發生。研究團隊開發出了一種能夠反映MYCN基因表現間距分佈的「空間特徵評分」,可用於預測肝癌發病風險。通過早期干預,將有望改善肝癌患者的預後並提升其生活品質(QOL)。相關研究成果已發表在《PNAS(美國科學院院刊)》的2月18日刊上。
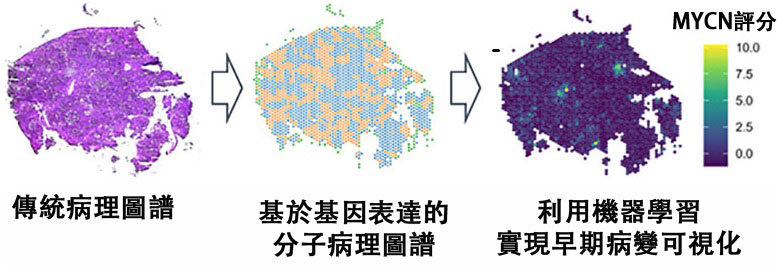
圖1 研究概念圖(供圖:理化學研究所)
2020年全球肝癌死亡人數超過83萬人,過去20年間增長了約1倍。據報告,肝癌治療後5年內的復發率高達79%,因此開發早期發現和預防技術已成為當務之急。
肝臟由肝實質細胞(肝細胞)及其餘非實質細胞(免疫細胞、纖維母細胞、血管構成細胞等)構成,這些細胞之間形成了一個相互作用複雜的「微環境」。在慢性肝損傷中,肝細胞的壞死與病理性再生反復發生,導致整個肝臟轉變為促進癌症發生的微環境,由此引發多片見性復發,即多個部位發生癌症。
此前,研究團隊一直在致力於探索決定非環狀類視黃醇抑制肝癌復發反應性的候選因子,並確定了癌基因MYCN是非環狀類視黃醇的靶點。此外,還開發了血液中MYCN定量檢測方法,並證實血液中MYCN可作為篩選對非環狀類視黃醇有反應患者的生物標誌物。雖然MYCN基因本身沒有突變,MYCN在肝癌幹細胞中的特異性表達水平與肝癌的惡性程度相關。另一方面,已知MYCN基因在正常肝臟中的表達水平較低,而在肝臟再生時,特別是在部分切除術後48小時的活躍肝細胞分裂期,其表達會呈現一過性峰值。
因此,本次研究旨在通過闡明肝癌微環境中的MYCN基因動態及其調控機制,驗證是否能夠區分生理性肝再生與病理性肝癌發生。
首先,研究人員將MYCN基因導入小鼠肝臟,並確認其可促進肝腫瘤的形成。
隨後,通過空間轉錄組學分析,追蹤了肝癌模型小鼠肝組織中MYCN基因表現的空間時間變化,並鑑定出具有肝癌幹細胞樣特徵信號的MYCN高表達區域。
該區域的出現頻率隨癌變過程增加,且在空間上與肝癌腫瘤標誌物Afb的高表達區域相鄰。在MYCN微環境中,確認了參與維持癌肝細胞性質的通路的顯著激活。周圍還觀察到了巨噬細胞的聚集。
此外,研究發現發炎性巨噬細胞的培養上澄液可在肝細胞中誘導MYCN表達,而肝細胞中MYCN的過度表達則會降低其對巨噬細胞刺激的反應性。這表明MYCN表達與發炎反應之間存在相互影響的反饋調控機制。同時,研究團隊還利用機器學習演算法開發了「MYCN評分」,用於量化MYCN微環境的空間特徵。
將該計算公式應用於人類肝細胞系的基因表現數據庫後,發現非腫瘤組織中的MYCN評分與肝癌復發風險存在強相關。研究表明,若非腫瘤組織中存在類似MYCN的致癌微環境,則未來肝癌復發的可能性較高。
秦高級研究員表示:「包括肝癌在內的上皮性腫瘤的發生,是由微環境中多種因子的複雜相互作用引起的,但其全貌一直難以掌握。本研究通過結合空間組學與機器學習,成功對肝癌微環境的整體狀況進行了定量評估。今後,我們將進一步推進空間特徵評分作為生物標誌物的臨床應用,同時闡明機器捕捉到的計算公式所揭示的肝癌發病本質。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Proceedings of the National Academy of Sciences of the United States of America(PNAS)
論文:Oncogenic function and transcriptional dynamics of MYCN in liver tumorigenesi
DOI:10.1073/pnas.2521923123