國立研究開發法人日本醫療研究開發機構(AMED)正在實施一項啟動與2024年,為期5年的「智慧生物製藥研究支援事業」項目。為推動日本自主研發出創新型生物藥品,該項目以「升級至臨床試驗」為目標。目前共有19個下屬項目正在推進,我們將分多期介紹這些具備開發潛力的「生物藥品原石」。

圖1 廣島大學研究生院醫系科學研究科岡田賢教授(供圖:廣島大學)
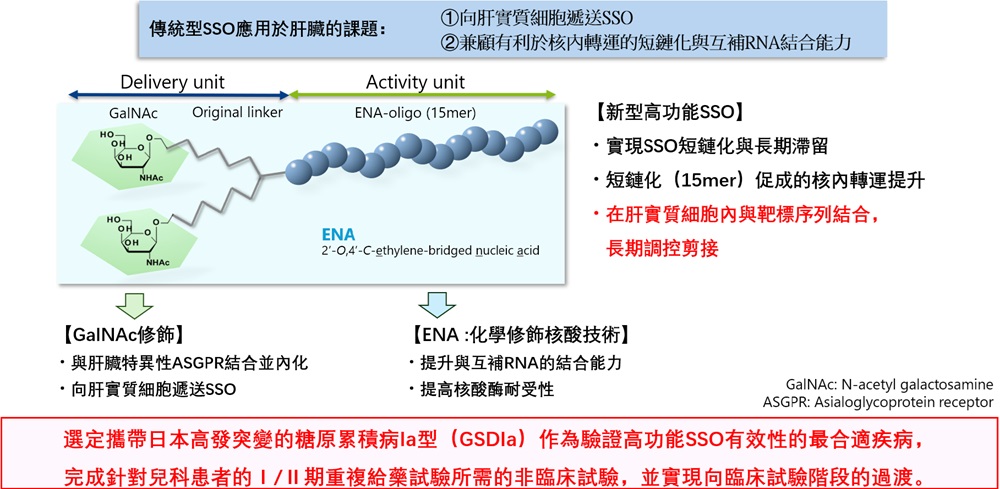
圖2 新型高功能剪接調控核酸(SSO)的實用化(供圖:廣島大學)
近年來,調節基因功能的剪接調控核酸(splice-switching oligonucleotide, SSO)已實現實用化,對既往難以治療的疾病也逐步展現出劃時代的治療效果。我們在既往研究中,通過結合肝實質細胞高效遞送技術(GalNAc修飾)與具備對互補RNA高結合能力及優異體內穩定性的化學修飾核酸技術(ENA),開發出了可在肝臟中實現強效且持續剪接調控的新型高功能SSO。本智慧生物製藥研究支援事業中,我們將該技術應用於攜有日本高發突變的肝醣累積病Ia型(glycogens torage disease type Ia, GSDIa)。
GSDIa是一種先天性代謝異常疾病,因編碼肝臟中負責將肝醣轉化為葡萄糖的酶——葡萄糖-6-磷酸酶(G6Pase)的G6PC基因存在功能缺陷,進而引發肝醣在肝臟蓄積所致的肝腫大,以及血糖降低所致的低血糖。肝腫大在幼年期即可出現,未來有可能進展為肝癌,因此需要從早期開展適當管理,但目前尚無有效治療方法。此外,低血糖在嬰幼兒期尤其易發展為重症,存在誘發中樞神經障礙的風險,因此以頻繁攝入高碳水化合物飲食為核心的嚴格飲食療法成為標準治療方案。然而,該療法不僅給患者及其家屬帶來沉重的身心負擔,即便在嚴格管控下也難以完全避免低血糖發作。此外,由低血糖引發的繼發性代謝異常及肝臟病灶多數並未得到充分改善,目前亟待開發根本性治療方法。
GSDIa為常染色體隱性遺傳,在日本患病率約為1/10萬,屬於罕見代謝性疾病,已被列為指定疑難病。該病存在種族特異性高發突變,東亞地區以G6PC基因c.648G>T突變最為多見(患者等位基因頻率:日本人群91%、韓國人群75%、中國人群54%)。該突變可引發剪接異常,進而造成G6Pase活性消失。我們認為通過新型高功能SSO矯正該剪接異常,有望實現對GSDIa的根本性治療,因此開展本研究。
截至目前,我們通過使用自主建立的GSDIa模型小鼠(c.648G>T突變敲入小鼠)開展研究,已發現了一種展現出顯著治療效果,且在最長3個月的給藥期內未觀察到重大安全性隱患的潛力SSO(Ito K, etal. J Clin Invest., 2023)。本項目旨在將該SSO創製為針對GSDIa的劃時代新藥,完成針對兒科患者的Ⅰ/Ⅱ期重複給藥試驗所需的非臨床試驗,並過渡至臨床試驗階段。以成人患者為對象的Ⅰ/Ⅱ期單次給藥試驗所需的非臨床試驗已完成,今後將推進試驗藥物的製造、幼齡小鼠試驗、生殖毒性試驗、長期毒性試驗以及臨床試驗方案的制定。通過本項目,我們將在驗證該技術臨床有效性與安全性的同時,推動向企業的技術輸出,致力於實現針對目前尚無根本療法的GSDIa的革新性治療藥物的實用化。
原文:《科學新聞》
翻譯:JST客觀日本編輯部