日本京都大學iPS細胞研究所(CiRA)臨床應用部門的山城春華(研究當時為研究生,現為醫學研究科助教)、小西聰史特定據點助教、後藤慎平教授等人組成的研究團隊宣佈,已鑑定出在人iPS細胞分化為氣道上皮多纖毛細胞過程中出現的前驅細胞「deuterosomal細胞」的特異性表面標誌物。同時還闡明瞭疑難病「纖毛不動症候群(PCD)」部分病型的發病機製,上述成果將有助於PCD診斷方法與治療方法的開發。相關研究內容已發表在《Stem Cell Reports》的3月19日刊上。
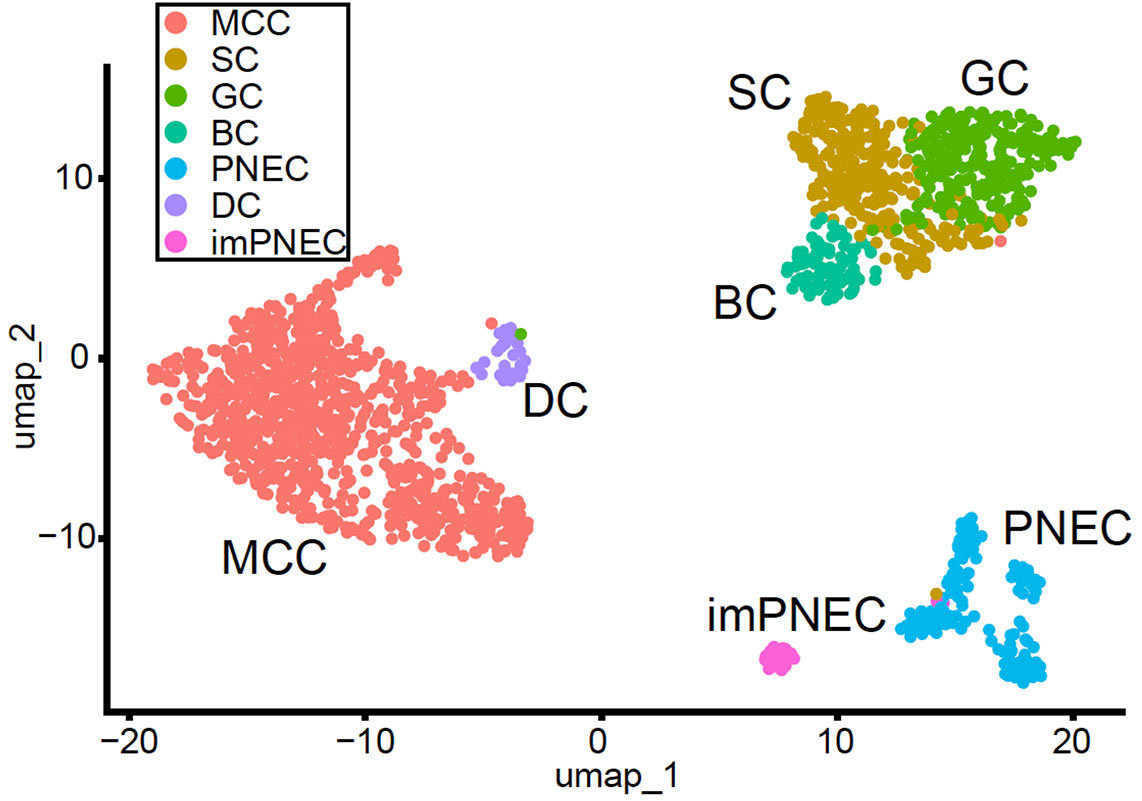
圖1 基於人類iPS細胞來源氣道上皮細胞scRNA-seq的UMAP分析(供圖:京都大學iPS細胞研究所)
每個點代表一個細胞,顯示位置越近的細胞性質越相似。確認存在deuterosomal細胞(DC)群。
氣道上皮細胞由多纖毛細胞等多種細胞構成,可將吸入的病原體與異物隨黏液一同排出,承擔著呼吸道防禦功能。該功能異常會引發以PCD為代表的慢性呼吸道感染。PCD是由纖毛相關基因突變導致的遺傳性疾病,發病率約為兩萬分之一,估算日本國內患者約有5000人,目前尚無有效療法。雖然此前已報告了多個致病基因,但大多與纖毛結構、運動相關,而與分化相關的研究仍十分有限。
在PCD中,纖毛數量減少的RGMC病型被認為是由參與纖毛分化的基因突變引起,其病因是CCNO基因突變導致。該基因被認為與纖毛的前身結構——中心粒的擴增有關,但詳細機制此前一直不清楚。
研究團隊聚焦於擴增途徑之一——通過大量產生中心體的「deuterosome依賴途徑」。纖毛由名為中心體的結構擴增形成,隨後向細胞頂端(表面方向)移動,並成熟為纖毛基部的基底小體。
Deuterosome是作為中心體支架的結構,擁有該結構的多纖毛細胞前驅細胞(deuterosomal細胞)僅在發育與再生過程中短暫出現,因此此前難以進行詳細解析。
為此,研究團隊利用此前已建立的從人iPS細胞誘導氣道上皮細胞的技術,通過單細胞轉錄成分析,鑑定出deuterosomal細胞,並確認該細胞在分化初期短暫達到峰值,之後逐漸轉變為成熟的多纖毛細胞的過程。
此外,研究團隊還發現了在該細胞中特異性表達的蛋白質CD36,並將其作為標記物分離出細胞。研究還證實,分離出的細胞中相關基因表現量高,向多線毛細胞分化能力強。
另外,還構建了攜帶CCNO突變的PCD患者來源iPS細胞,以及修復了該突變的iPS細胞,分別誘導分化為氣道上皮細胞並進行比較分析。
結果顯示,疾病特異性iPS來源的氣道上皮細胞中CCNO蛋白表達下降,多纖毛細胞形成顯著受損。相比之下,基因修復後的iPS細胞來源細胞則得到恢復,中心粒的數量也有所增加。這表明CCNO突變通過引起氣道中心粒擴增障礙,導致多纖毛形成障礙。
研究人員對疾病特異性iPS細胞及其修復型細胞誘導而來的氣道上皮細胞分別進行單細胞轉錄成分析,詳細比較了基因表現。
結果顯示,在修復iPS細胞中,經由deuterosomal細胞正常分化為多纖毛細胞;而在疾病特異性iPS細胞來源的氣道上皮細胞中,出現了不經過deuterosomal細胞的分化途徑,異常細胞群也隨之增加。
研究團隊表示,今後將利用以CD36為指標的分離方法,進一步深入理解對該疾病病理的理解。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Stem Cell Reports
論文:Deuterosomal cells are the responsible lineage for multiciliogenesis in human airway differentiation
DOI:10.1016/j.stemcr.2026.102860