神戶大學生物信號綜合研究中心的蜷川曉助教、松尾將生(碩士生),京都大學研究生院理學研究科的森和俊教授(研究當時)、鄧櫻(研究當時為碩士生)、自然科學研究機構生命創成探究中心的加藤晃一教授以及名古屋市立大學研究生院藥學研究科的矢木宏和副教授等組成的研究團隊宣佈,發現了蛋白質在內質網中的命運是通過糖鏈介導的結構形成因子和降解因子之間的「拔河」作用來決定的。這一發現得益於對內質網中促進蛋白質結構形成的糖鏈修飾酶「UGGT1」的功能研究。預計該研究成果將有望助力新型疾病治療和預防方法的開發。相關研究成果於2024年12月10日發表在國際學術期刊《eLife》上。
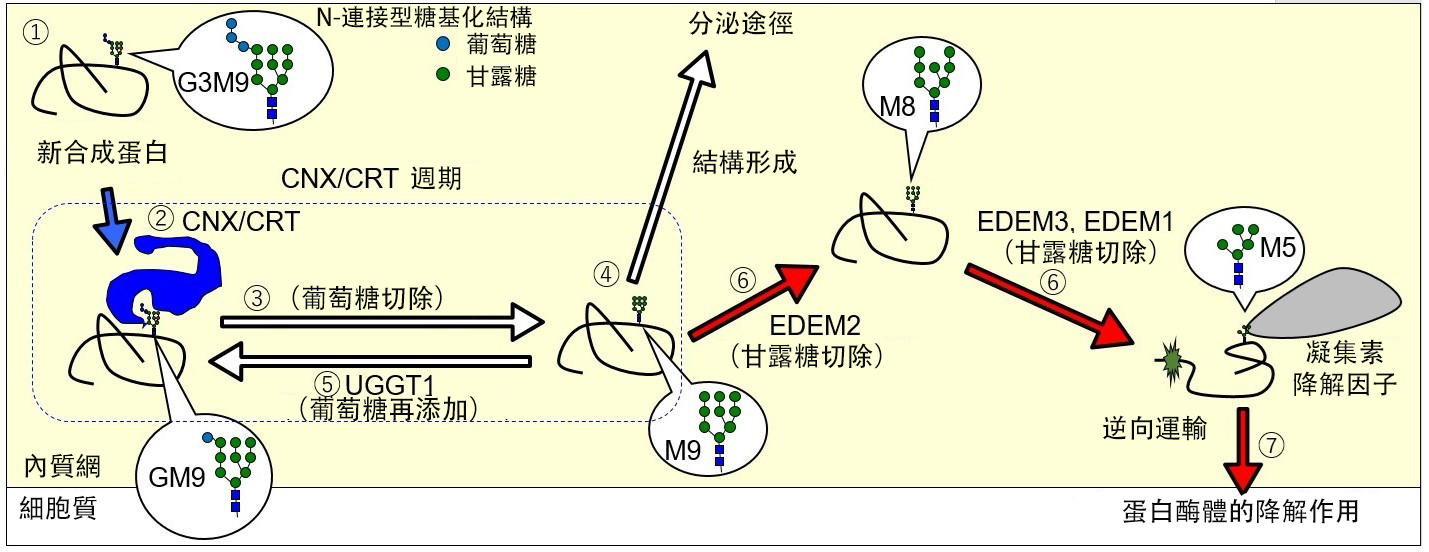
圖1以N型糖鏈為中心的內質網蛋白質品質管制機制概要圖(供圖:神戶大學)
內質網是細胞內的一個重要胞器,負責合成包括膜蛋白和分泌蛋白在內的分泌途徑蛋白質群在內的約三分之一的全蛋白質,其中約80%的蛋白質被添加了N型糖鏈,並通過這些糖鏈介導精密的品質管制機制。
此前的研究表明,內質網中蛋白質的結構和降解途徑因N型糖鏈的存在與否而有顯著差異。
N型糖鏈由三個葡萄糖(G)和九個甘露糖(M)(即G3M9)組成,通過切除糖基轉化為GM9後,其結構被獨特性分子伴侶CNX或CRT識別,進而促進蛋白質的結構形成。如果結構形成,則蛋白質繼續進入分泌途徑;如果結構未能形成,那麼糖基修飾酶UGGT1會重新附加葡萄糖,啟動新一輪循環。而當蛋白質始終無法形成結構時,EDEM2切除N型糖鏈中的甘露糖,最終被識別並導向分解。此前尚不清楚在這種機制中,蛋白質的命運是如何被決定的。
長期以來,UGGT1被認為僅與結構形成相關,對降解時機無直接影響,但這一點尚缺乏完全證明。
為驗證此假設,研究團隊製作了UGGT1基因剔除細胞(KO細胞)。
結果發現,在UGGT1-KO細胞中,與對照細胞相比,分解基質膜蛋白ATF6的N型糖鏈未重新附加葡萄糖,其分解顯著加速,表明糖鏈修飾酶UGGT1抑制了蛋白質的分解。
此外,UGGT1對結構穩定、半衰期長的蛋白質沒有明顯影響,但對結構不完整或不穩定的蛋白質,UGGT1能抑制其降解。
研究團隊總結了以往的研究結果,確定結構形成因子和降解因子的數量平衡決定了蛋白質趨向形成結構還是降解。通過糖鏈介導的結構形成和降解因子的「拔河」作用,決定了內質網中蛋白質的命運。
內質網功能與阿茲海默症、癌症和糖尿病等60多種人類疾病密切相關。此次研究成果為未來開發新療法及預防策略奠定了重要基礎。
蜷川助教表示:「很高興能夠解開小細胞本體的蛋白質在內質網中進行生物合成後,究竟是形成結構還是被降解這一命運決定機制,這是一個極其重要的過程。特別是發現原本被認為完全不參與分解過程的UGGT1竟然能夠顯著抑制ATF6及其他不穩定蛋白的分解,這一結果讓我們感到十分驚訝。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:eLife
論文:UGGT1-mediated reglucosylation of N-glycan competes with ER-associated degradation of unstable and misfolded glycoproteins
DOI:10.7554/eLife.93117