東京科學大學綜合研究院細胞控制工學研究中心的博士生李子洋(研究當時)和中戶川仁教授等人的研究團隊,成功解明瞭因細胞核自噬(選擇性降解細胞核的自噬途徑,即細胞核自噬)失調而導致細胞死亡的機制。相關研究成果已發表在期刊《Nature Communications》上。
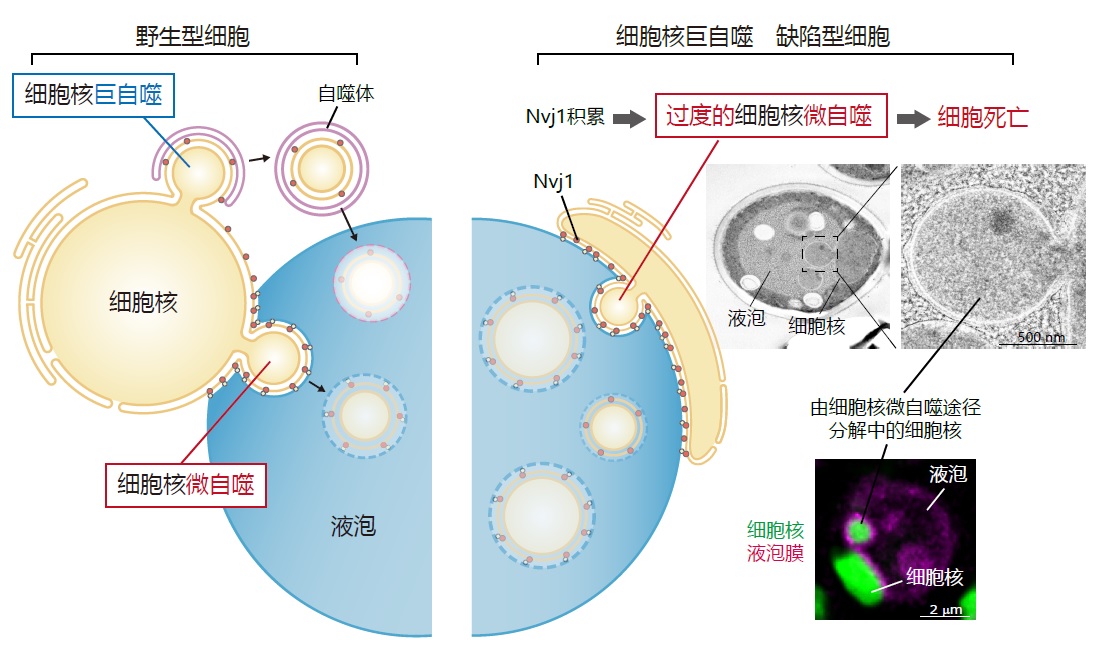
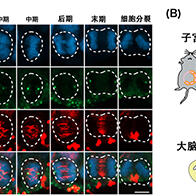
圖1 闡明瞭由於細胞核巨自噬(一種降解部分細胞核的自噬途徑)失調而引發細胞死亡的機制。當細胞核巨自噬停止時,細胞核微自噬被過度激活,從而導致細胞死亡(供圖:東京科學大學)
在酵母細胞中,細胞核自噬存在「巨自噬」和「微自噬」兩種途徑。微自噬過程中,溶體或液泡的膜向內凹陷,將待分解的物質直接包裹並降解。而巨自噬則通過自噬小體(一種膜結構)先包裹降解目標,然後運送至溶體或液泡進行分解。
研究團隊此前的研究表明,酵母細胞主記憶體在一種通過巨自噬降解細胞核的選擇性機制,即細胞核巨自噬(Macro-Nucleophagy)。細胞核是負責儲存和克隆基因體DNA並執行基因表現的關鍵胞器,而在細胞核巨自噬的過程中,Atg39蛋白介導細胞核部分區域被自噬小體包裹,並最終在液泡內降解。
敲除Atg39蛋白的細胞在營養匱乏環境下會出現細胞核形態異常,並比野生型細胞更早降低存活率,這表明細胞核巨自噬對適應營養缺乏至關重要。然而,為什麼在營養匱乏時需要降解部分細胞核?以及細胞核巨自噬的停止如何引發細胞核形態異常和生存率下降?這些問題仍然未解。
研究團隊利用螢光成像分析發現,在營養匱乏狀態下,Atg39敲除細胞的細胞核巨自噬停止時,細胞核內容物會形成巨大結構體並被液泡內吞。在此過程中,液泡膜向內凹陷,將來自細胞核的結構體吞入液泡內部。進一步研究發現,敲除細胞核微自噬所需的Nvj1蛋白時,這一吞噬過程被阻斷,這說明細胞核巨自噬的停止會導致細胞核微自噬的過度亢進。
核膜蛋白Nvj1在營養匱乏狀態下,會被Atg39依賴性的細胞核巨自噬所降解,在此次研究的Atg39敲除細胞中,Nvjl大量積累導致了細胞核微自噬被過度激活。這表明在正常細胞中,細胞核巨自噬抑制了細胞核微自噬的失控。進一步的研究證實,當通過敲除Nvj1來使過度激活的細胞核微自噬停止時,Atg39敲除細胞中的細胞核形態異常和存活率下降的情況幾乎完全恢復。換言之,該研究證明了細胞核巨自噬的停止會導致細胞核微自噬的異常活化,甚至產生致命影響;而抑制細胞核微自噬過度活化是細胞核巨自噬的重要功能之一。
相對於出芽酵母的細胞核(直徑約1.5~2微米),細胞核巨自噬所降解的部分很小(小於0.15微米),而失控的細胞核微自噬所降解的部分非常大,直徑可超過1微米,甚至包含DNA結合蛋白和核小體蛋白。因此,當細胞核微自噬失控時,可能造成細胞生存所必需的關鍵核成分被液泡吞噬,影響細胞的基本存活功能;或可致核內基因表現受損,使細胞無法適應營養匱乏的環境,最終走向死亡。
此次研究揭示了細胞核自噬失控與細胞死亡之間的關係,表明受控的細胞核自噬對細胞穩定狀態至關重要。該發現不僅為理解自噬相關疾病提供了基礎資訊,也為未來的疾病研究和干預策略奠定了科學基礎。
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Nature Communications
論文:Macronucleophagy maintains cell viability under nitrogen starvation by modulating micronucleophagy
DOI:10.1038/s41467-024-55045-9