岐阜大學高等研究院的特任助教東小百合和德國明斯特大學的Seraphine V. Wegner教授等人組成的研究團隊發表研究結果稱,確立了控制巨型微脂體中金屬酶活性的技術,並成功開發出了響應外部金屬離子的刺激而改變命運的人造細胞。該技術將有助於設計模擬細胞分化的「多能性人造細胞」。相關研究成果已發表在國際期刊《Nature Chemistry》2024年12月23日刊上。
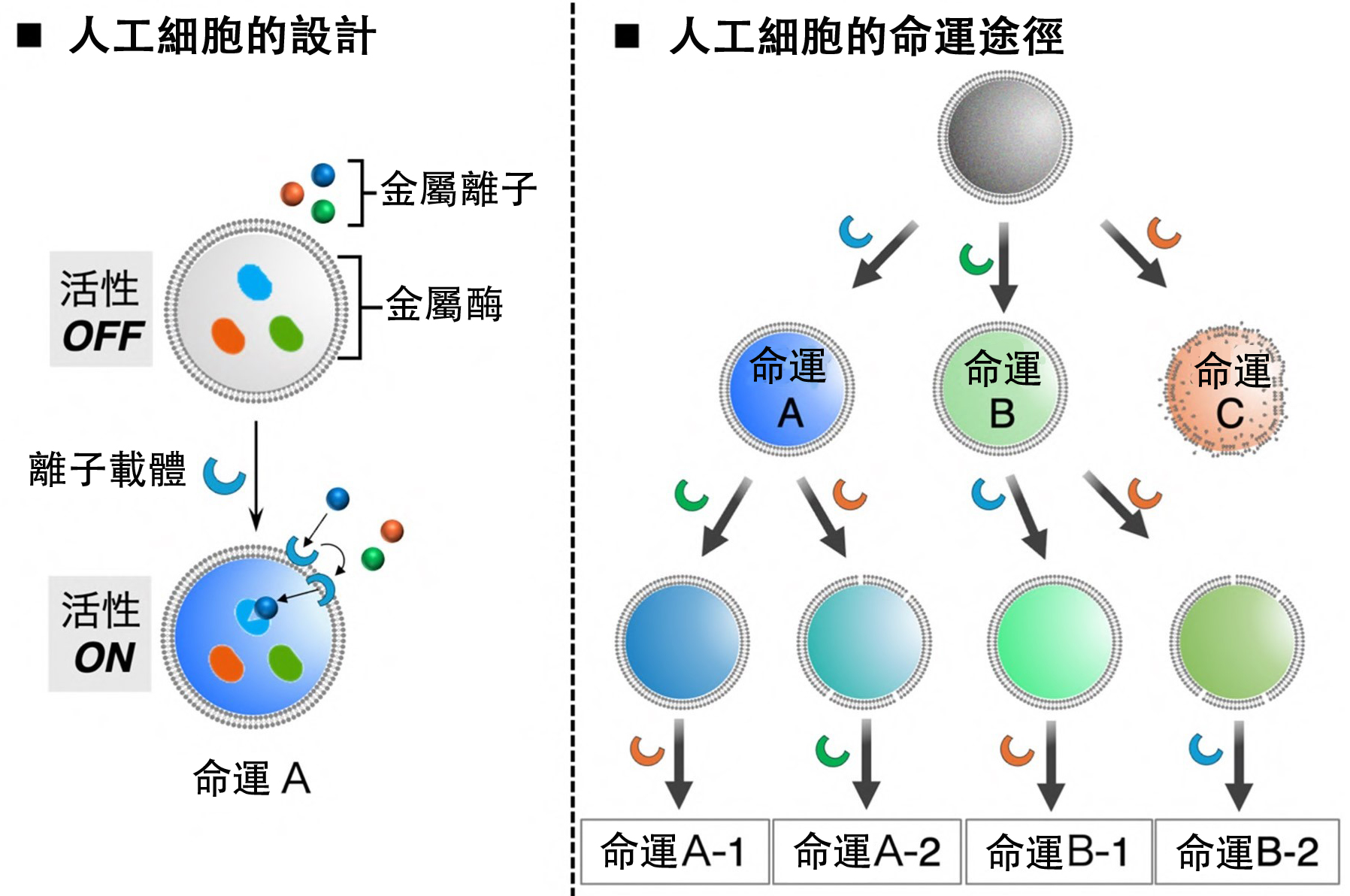
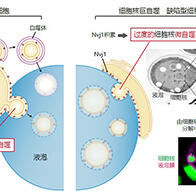
圖1 研究概念圖(供圖:岐阜大學)
近年來,人們一直為瞭解細胞現象及其在生物材料中的應用而進行人工製造細胞的研究。為了模擬細胞的功能,人們開發出瞭如基因表現(克隆、轉錄和翻譯)、生成ATP(三磷酸腺)、由多種酶反應組成的新陳代謝、細胞分裂和融合、細胞間粘附和資訊傳遞等具有重要基礎功能的人造細胞。另一方面,大多數現有的人造細胞隻注重於其中的一種功能,並被設計為響應外界刺激來表達功能。兼具多種功能的人造細胞此前一直未被開發出來。
另一方面,研究團隊一直致力於開發巨型微脂體(GUV),並將其作為細胞膜來包裹生物分子,以此來進行開發人造細胞的研究。
此次,研究團隊的目標是利用人造細胞來模仿細胞的適應力,開發出響應3種不同刺激的人造細胞。
在細胞中,將外部刺激正確傳遞到內部的機制非常重要,而在細胞膜上表達的轉運體、通道和接受者等膜蛋白會轉運或結合不能通過細胞膜的物質,從而產生各種反應(細胞現象)。
因此,研究人員將向內部傳遞特定刺激的轉運體與人造細胞膜結合,並將3種不同功能的金屬依賴性酶封裝在用作細胞膜模型的細胞大小的微脂體GUV內。通過與細胞膜結合的離子載體(提高特定金屬離子的膜滲透性的分子群)所進行的金屬離子轉運來控制各種金屬酶的活性。
事實證明,在人造細胞外部3種金屬離子共存的環境中,將特定的離子載體結合到細胞膜上,會根據離子載體的選擇表現出不同的功能。
研究還發現,同時將3種離子載體與細胞膜結合會同時抑制任一種金屬離子的轉運。
分子動力學模擬的結果表明,細胞膜內離子載體之間的相輔作用可能會抑制它們在細胞膜上的移動,阻礙金屬離子的轉運。
此外,將3種離子載體按不同順序與細胞膜結合後發現,與較晚結合到細胞膜上的離子載體相對應的金屬酶的活性水平明顯降低。由此可見,離子載體與細胞膜結合的順序會影響金屬酶的活性水平。
東特任助教表示:「該研究主要是我在德國明斯特大學韋格納實驗室留學期間進行的。在嘗試利用巨型微脂體、金屬酶和離子載體開發人造細胞模型的過程中,我經歷了許多困難,也學到了很多。特別是將金屬酶封裝在巨型微脂體中時,花費了六個多月的時間才找到去除和滅活金屬離子的最佳條件。未來,我希望利用金屬離子相關的各種蛋白質,繼續開發功能性人造細胞。」
原文:《科學新聞》
翻譯:JST客觀日本編輯部
【論文資訊】
期刊:Nature Chemistry
論文:Adaptive Metal Ion Transport and Metalloregulation-Driven Differentiation in Pluripotent Synthetic Cells
DOI:10.1038/s41557-024-01682-y